
【题目】在容积不变的密闭容器中,一定条件下发生反应:2A![]() B(g)+2C(g),且达到平衡。当升高温度时气体的密度增大,则下列叙述中正确的是
B(g)+2C(g),且达到平衡。当升高温度时气体的密度增大,则下列叙述中正确的是
A.升高温度,正反应速率增大,逆反应速率减小
B.若正反应是放热反应,则A为气态
C.若向容器中充入惰性气体,则平衡向右移动
D.物质A一定为非气态,且正反应是吸热反应
【答案】D
【解析】
A项无论该反应是吸热反应还是放热反应,升高温度,正逆反应速率都增大,故A错误;
B项若正反应是放热反应,升高温度平衡向逆反应方向移动,容器内气体的密度增大,说明气体的质量增大,则A一定为非气态才符合,故B错误;
C项、若向容器中充入惰性气体,虽然容器的压强增大,但不改变参加反应气体的浓度,所以平衡不移动,故C错误;
D项、因为容器的体积固定,如果A是气体,升高温度时,无论平衡向哪方向移动,气体的密度始终不变,则A一定是非气体,且升高温度,平衡向正反应方向移动时气体的密度才增大,所以正反应是吸热反应,故D正确;
故选D。
【点晴】
解答本题的关键是容器密度的变化,达到化学平衡后,升高温度,容器内气体的密度增大,说明气体的质量增大,要使气体的密度增大,根据ρ=m/V知,A一定为非气态,对于容器体积固定的可逆反应,惰性气体不影响平衡的移动,但温度一定影响反应速率,据此分解作答。


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
【题目】25℃下,现有0.1mol·L-1的H2SO4和0.1 mol·L-1一元弱酸HA两种溶液
(1)实验测得0.1 mol·L-1一元弱酸HA 的pH为4,则HA的电离平衡常数Ka= ;
(2)0.1mol·L-1的H2SO4中水电离出的C(H+)为 ;
(3)向0.1mol·L-1的硫酸中加入一定体积的pH=13的NaOH溶液,反应后溶液的pH为2,则所需NaOH溶液与硫酸的体积比为 ;
(4)向0.1 mol·L-1一元弱酸HA加入一定体积的水,在此过程中,下列数值变大的是 ;
①c(H+) ② 电离度(α) ③c(OH-) ④ Ka ⑤c(A-)/ c(HA) ⑥n(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的锌与![]() 的浓硫酸充分反应后,锌完全溶解,同时生成气体
的浓硫酸充分反应后,锌完全溶解,同时生成气体![]() 标准状况下测定
标准状况下测定![]() 。将反应后的溶液稀释至1L,测得溶液中
。将反应后的溶液稀释至1L,测得溶液中![]() ,则下列叙述中错误的是( )
,则下列叙述中错误的是( )
A.反应中消耗的Zn的质量为![]() B.反应中被还原的元素有两种
B.反应中被还原的元素有两种
C.气体A中![]() 和
和![]() 的体积比为3:4D.反应中共转移电子3mol
的体积比为3:4D.反应中共转移电子3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的CuS和![]() 的混合物投入足量的
的混合物投入足量的![]() 中,收集到气体
中,收集到气体![]() 标准状况
标准状况![]() ,向反应后的溶液中
,向反应后的溶液中![]() 存在
存在![]() 和
和![]() 加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到
加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到![]() ,若上述气体为NO和
,若上述气体为NO和![]() 的混合物,且体积比为
的混合物,且体积比为![]() ,则V可能为
,则V可能为![]()
![]()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.Na2S 溶液的水解:S2-+ 2H2O ![]() H2S + 2OH-
H2S + 2OH-
B.NaHCO3 溶液的电离:HCO3-+ H2O ![]() H2CO3+ OH-
H2CO3+ OH-
C.NH4Cl 溶液的水解:NH4++ H2O ![]() NH3·H2O+ H+
NH3·H2O+ H+
D.水溶液中的 NaHSO4 电离:NaHSO4=Na++HSO4-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.工业合成氨反应在生产中具有重要意义,完成下列问题:
(1)写出合成氨反应的热化学方程式:____。
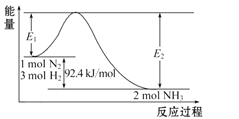
(2)在甲乙两个体积均为 2L 固定容积的密闭容器中,分别充入甲:1molN2、3molH2 和乙:2molN2、6molH2(其它条件相同),经过足够长的时间后,在乙容器中放出热量_____________ (填“大于”、 “小于”或“等于”)在甲容器中放出热量的 2 倍。
(3)下列图像分别代表焓变(△H)、混合气体平均相对分子质量(![]() )、N2 体积分数 φ(N2)和气体密度(ρ)与反应时间关系,其中正确且能表明该可逆反应达到平衡状态的是_____________ 。
)、N2 体积分数 φ(N2)和气体密度(ρ)与反应时间关系,其中正确且能表明该可逆反应达到平衡状态的是_____________ 。
A. 
B. 
C. 
D. 
Ⅱ.常温下,有浓度均为 0.1 mol·L-1 的下列 4 种溶液:①H2SO4 溶液②CH3COOH 溶液③Na2CO3 溶液④NaOH 溶液
(1)以上 4 种溶液 pH 由大到小的排列顺序是______________(填序号),其中由水电离出的H+浓度最小的是____________ (填序号)。
(2)③溶液中离子浓度由大到小的顺序____________。
(3)该温度下向②中加入少量 CH3COONa,此时![]() 的值____________(填“增大”、“减小”或“不变”)。
的值____________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+2B(g) ![]() C(g)的能量变化与反应进程关系如图所示,下列说法不正确的是( )
C(g)的能量变化与反应进程关系如图所示,下列说法不正确的是( )

A.图中虚线表示加入了催化剂
B.图中虚线表示的反应I、反应II均为放热反应
C.加入催化剂,速率加快是因为改变了反应的焓变
D.该反应的焓变△H=-91kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是人类赖以生存的基础。回答下列问题:
(1)下列不属于新能源的是___(填字母)。
a.煤炭 b.太阳能 c.风能 d.地热能 e.天然气 f.氢能
(2)甲烷裂解法制取乙炔反应的化学方程式为2CH4(g)![]() C2H2(g)+3H2(g)。
C2H2(g)+3H2(g)。
①已知下列化学键的键能数据:
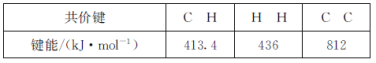
则反应2CH4(g)![]() C2H2(g)+3H2(g)的△H=___kJ·mol-1。
C2H2(g)+3H2(g)的△H=___kJ·mol-1。
②燃烧agCH4生成二氧化碳气体和液态水,放出热量44.5kJ。经测定,生成的CO2与足量澄清石灰水反应得到5g沉淀,则CH4(g)+2O2(g)![]() CO2(g)+2H2O(l)△H1=___kJ·mol-1,a=___。
CO2(g)+2H2O(l)△H1=___kJ·mol-1,a=___。
(3)金刚石和石墨为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时完全燃烧生成二氧化碳,反应中放出的热量如图所示。

①在通常状况下,金刚石和石墨的稳定性较大的是___(填“金刚石”或“石墨”);石墨的燃烧热为___kJ·mol-1。
②12g石墨在-定量空气中燃烧,生成36g气体,该过程放出的热量为___kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示正确的是( )
A.次氯酸的电离方程式:HClO=H++ClO-
B.只有熵增加的过程才能自发进行
C.HS-水解离子方程式:HS-+H2O![]() H3O++S2-
H3O++S2-
D.已知中和热为57.3 kJ·mol-1,稀硫酸与氢氧化钠稀溶液反应的热化学方程式:H2SO4 (aq)+2NaOH (aq)== Na2SO4 (aq)+2H2O ( l ) ΔH=-114.6 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com