
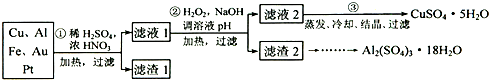
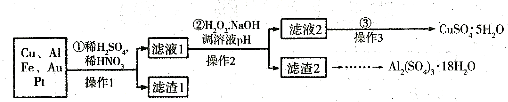
��Ϣʱ�������Ĵ������������Ի�������˼������в��ij�����Ϊ����ѧ��̽��С�齫һ����������·������õ���70%Cu��25%Al��4%Fe������Au��Pt�Ƚ����Ļ�������Ƴ������Ʊ�����ͭ�����·�ߣ�

�ش��������⣺
�ŵڢٲ�Cu���ᷴӦ�����ӷ���ʽΪ ���õ�����1����Ҫ�ɷ�Ϊ ��
�Ƶڢڲ�����H2O2�������� ��ʹ��H2O2���ŵ��� ������pH��Ŀ����ʹ ���ɳ�����
���õڢ۲�����CuSO4��5H2O�Ʊ���ˮCuSO4�ķ����� ��
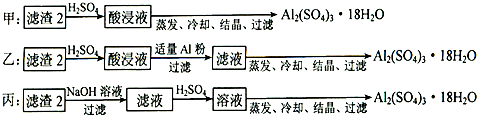
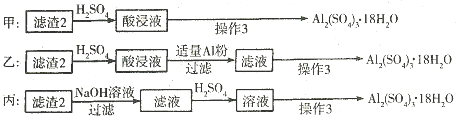
��������2��ȡAl2(SO4)3��18H2O��̽��С����������ַ�����
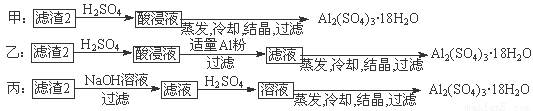
�������ַ����У� ���������У�ԭ���� ��
��ԭ�������ʽǶȿ��ǣ� ������������
��̽��С���õζ����ⶨCuSO4��5H2O(Mr=250)������ȡa g �������100 mL��Һ��ÿ��ȡ20.00 mL�������������Ӻ���c mol/L EDTA(H2Y2��)����Һ�ζ����յ㣬ƽ������EDTA��Һb mL���ζ���Ӧ���£�Cu2++ H2Y2����CuY2��+ 2H+
д������CuSO4��5H2O���������ı���ʽ�أ� ��
���в����ᵼ��CuSO4��5H2O�����ⶨ���ƫ�ߵ��� ��
a��δ������ƿ
b���ζ��յ�ʱ�ζ��ܼ����в�������
c��δ��������EDTA��Ӧ�ĸ�������
��Cu��4H����2NO3�� Cu2����2NO2����2H2O��3Cu��8H����2NO3��
Cu2����2NO2����2H2O��3Cu��8H����2NO3�� 3Cu2����2NO����4H2O��Au��Pt
3Cu2����2NO����4H2O��Au��Pt
�ư�Fe2������ΪFe3�������������ʣ�����Ի���������Ⱦ��Fe3����Al3����
���������м�����ˮ
�ȼף�������������ֻ�����������������������������ȴ���ᾧ�����˵õ��������������л��д������������ʣ��ҡ�
��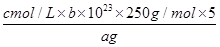 ��100%��c��
��100%��c��
��������
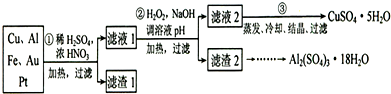
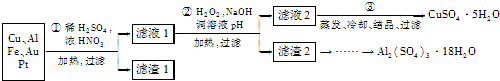
�����������1��Ũ������ϡ�����ϣ��������ΪŨ��Һ��Ҳ����Ϊϡ��Һ�������������ӷ���ʽ���ɣ�Au��P���������ᷴӦ����������1����Ҫ�ɷ�Ϊ��Au��Pt��
��2���ڢڲ���H2O2�������ǰ�Fe2������ΪFe3����H2O2�����������仹ԭ����ΪH2O�����Ը����������ŵ��Dz��������ʣ�����Ի���������Ⱦ������ҺPH��Ŀ����ʹFe3����Al3���γɳ�����
��3���ڢ۲�����ˮ����ͭ�Ʊ�����ͭ�ķ���Ӧ���������м�����ˮ��
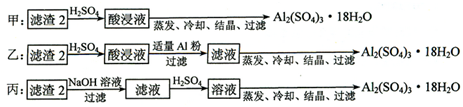
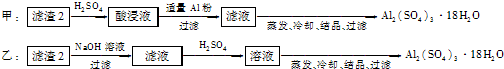
��4���Ʊ�����������ļס��ҡ������ַ����У�������������ֻ�����������������������������ȴ���ᾧ�����˵õ��������������л��д������������ʣ����������С��Һͱ����������С��ҷ������������м�H2SO4������Fe2(SO4)3��Al2(SO4)3,�ټ�Al�ۺ�Fe2(SO4)3����Al2(SO4)3,��������ȴ���ᾧ�����˿ɵ����������塣���������������м�NaOH,��Al(OH)3��Ӧ����NaAlO2��������Һ�м�H2SO4����Al2(SO4)3, ��������ȴ���ᾧ�����˿ɵ����������塣����ԭ�����ýǶȿ��Ƿ����Ҹ���������Ϊ���ӵ�NaOH���Ʊ���Al2(SO4)3��ԭ�����û�й�ϵ�����ԭ���˷ѡ�
��5���������ӷ���ʽ��Cu2+�����ʵ�������EDTA�����ʵ�����������EDTA�����ʵ��������CuSO4•5H2O�����ʵ�������Ϊ������100mL CuSO4��Һ��ÿ��ȡ20.00mLʵ�飬�����ٳ���5���ɵ���Ʒ��CuSO4•5H2O�����ʵ������������CuSO4•5H2O�ĺ�����a��δ������ƿ��Ϊ��ȷ��������Ӱ��ṹ��b���ζ��յ�ʱ�ζ��ܼ����в������ݣ�ʹ��Һ���������ֵ��С���ṹƫС��c��δ��������EDTA��Ӧ�ĸ������ӣ�������EDTA��������ʹ���ƫ�ߡ�
���㣺���⿼�����ӷ���ʽ����д���Լ������á�ʵ�鷽���ķ������к͵ζ��ļ�������ķ�����


 ʱ�����������ҵԭ���ܳ�����ϵ�д�
ʱ�����������ҵԭ���ܳ�����ϵ�д� ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ||
| ||
| ||
| ||

| c mol?L-1��b��10-3L��250g?mol-1��5 |
| ag |
| c mol?L-1��b��10-3L��250g?mol-1��5 |
| ag |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ������ | Fe��OH��2 | Fe��OH��3 | Al��OH��3 | Cu��OH��2 |
| ��ʼ���� | 5.8 | 1.1 | 4.0 | 5.4 |
| ��ȫ���� | 8.8 | 3.2 | 5.2 | 6.7 |
2- 3 |
2- 6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com