
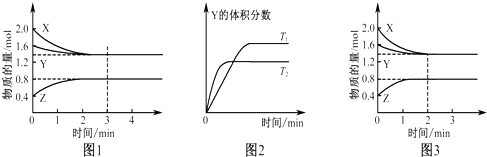
| A、反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol/(L?min) |
| B、平衡时容器内的压强为反应前的0.9倍 |
| C、保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| D、若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
| △c |
| t |
| △c |
| t |
| ||
| 3 |
| 3.6 |
| 4.0 |


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
| A、盐酸、氢氧化钠溶液、石蕊试液 |
| B、盐酸、氢氧化钠溶液、酚酞 |
| C、氢氧化钠溶液、氢氧化钡溶液、硫酸 |
| D、硫酸铜溶液、盐酸、氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaNO3 (溶液) |
| B、CH3COONa(固体) |
| C、Na2CO3(溶液) |
| D、CuSO4 (固体) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4H受热分解属非氧化还原反应 |
| B、NH4H溶于水,所形成的溶液显碱性 |
| C、NH4H与水反应时,NH4H既是氧化剂又是还原剂 |
| D、NH4H与水反应时,水既不是氧化剂又不是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、图Ⅰ研究的是t0时刻增大O2的浓度对反应速率的影响 |
| B、图Ⅱ研究的是t0时刻加入催化剂后对反应速率的影响 |
| C、图Ⅲ研究的是催化剂对平衡的影响,且甲的催化效率比乙高 |
| D、图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、欲分离硝酸钾和氯化钠的混合物(物质的量比为1:1),先将样品溶解,然后加热至表面出现晶膜后再冷却,过滤得硝酸钾晶体;再将母液加热至大量晶体析出后,用余热蒸干,得氯化钠晶体 |
| B、摘下几根火柴头,浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸,若出现白色沉淀,就说明含有氯元素 |
| C、实验室制取肥皂:将适量植物油、乙醇和NaOH溶液混合,并不断搅拌、加热,直到混合物变稠,即可得到肥皂 |
| D、乙酸乙酯制备实验中,在粗产品中加入饱和Na2CO3溶液处理除去乙酸、乙醇等杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、制备气体前,先往装置中装入药品,后检查装置的气密性 |
| B、稀释浓硫酸时,先往容器中装水,后慢慢倒入浓硫酸并不断搅拌 |
| C、测定溶液的酸碱度时,先将pH试纸用水润湿,后沾上被测溶液 |
| D、做一氧化碳还原氧化铁的实验时,先加热、后通一氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素的化学性质与原子最外层电子数目关系密切 |
| B、原子是化学反应中最小的微粒,因此原子不可再分 |
| C、物质是由分子、原子、离子等粒子构成的 |
| D、核内质子数决定了元素的种类 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com