
【题目】研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为______________________。利用反应6NO2+8NH3 ![]() 7N2+12 H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是__________L。
7N2+12 H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是__________L。
2)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)的ΔH=_________kJ·mol、1。
SO3(g)+NO(g)的ΔH=_________kJ·mol、1。
一定条件下,将NO2与SO2以体积比1︰2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1︰6,则平衡常数K=__________________。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。
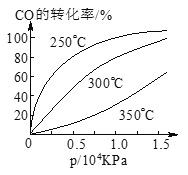
CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH___________0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是________________________。
【答案】3NO2+H20=HNO3+NO 6.72 -41.8 b
8/3 < 此压强下,一氧化碳转化率接近100%
【解析】
试题解析:(1)二氧化氮与水反应生成硝酸和一氧化氮;3NO2+H20=HNO3+NO;6NO2+8NH3 ![]() 7N2+12 H2O也可处理NO2。该反应转移电子24摩尔e-, 生成氮气7摩尔;当转移1.2 mol电子时,消耗的NO2在标准状况下1.2×7×22.4/24=6.72L; 2)根据盖斯定律,处理两个方程式,消去氧气,得到NO2(g)+SO2(g)
7N2+12 H2O也可处理NO2。该反应转移电子24摩尔e-, 生成氮气7摩尔;当转移1.2 mol电子时,消耗的NO2在标准状况下1.2×7×22.4/24=6.72L; 2)根据盖斯定律,处理两个方程式,消去氧气,得到NO2(g)+SO2(g)![]() SO3(g)+NO(g)的ΔH=-41.8 kJ·mol、1。达到平衡状态:a.反应前后为体积不变的反应,所以反应体系压强任何时候都保持不变;错误;b.混合气体颜色保持不变,即二氧化氮气体的浓度不变,达平衡状态;正确;c.SO3和NO为生成物,任何时候体积比都保持不变,无法确定;错误;d.每消耗1 mol SO3为逆反应速率,同时生成1 mol NO2为逆反应速率,方向相同,无法判断;错误;答案为b;测得上述反应平衡时NO2与SO2体积比为1︰6,
SO3(g)+NO(g)的ΔH=-41.8 kJ·mol、1。达到平衡状态:a.反应前后为体积不变的反应,所以反应体系压强任何时候都保持不变;错误;b.混合气体颜色保持不变,即二氧化氮气体的浓度不变,达平衡状态;正确;c.SO3和NO为生成物,任何时候体积比都保持不变,无法确定;错误;d.每消耗1 mol SO3为逆反应速率,同时生成1 mol NO2为逆反应速率,方向相同,无法判断;错误;答案为b;测得上述反应平衡时NO2与SO2体积比为1︰6,
NO2(g)+SO2(g)![]() SO3(g)+NO(g)
SO3(g)+NO(g)
起始 a 2a 0 0
变化 x x x x
平衡 a-x 2a- x x x
(a-x)/(2a-x)=1/6,x=4a/5;则平衡常数K=x2/(a-x)×(2a-x)=8/3;(3)CO(g)+2H2(g)![]() CH3OH(g)。压强不变,温度由350℃降到300℃,一氧化碳的转化率增大,平衡右移,正反应放热;ΔH《0;实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是此压强下,一氧化碳转化率接近100%;
CH3OH(g)。压强不变,温度由350℃降到300℃,一氧化碳的转化率增大,平衡右移,正反应放热;ΔH《0;实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是此压强下,一氧化碳转化率接近100%;


科目:高中化学 来源: 题型:
【题目】常温下c(H+)最小的是下列各项中的
A.pH=0的溶液
B.0.5 mol·L-1 H2SO4
C.0.5 mol·L-1 HCl
D.0.6 mol·L-1CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为二氧化锰的有关转化关系图,有关说法中不正确的是( )
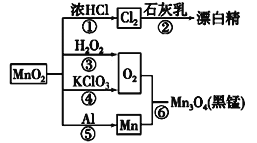
A.反应①~⑥均属于氧化还原反应
B.反应①中氧化剂与还原剂的物质的量之比为1∶4
C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶2
D.反应②中Cl2既是氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不属于垃圾资源化的是( )
A. 将垃圾填埋 B. 建立垃圾发电厂
C. 分类收集和回收利用废塑料 D. 回收旧电子产品并将其集中分拆处理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中,所用仪器合理的是( )
A. 在坩埚中放入NaCl溶液,加热、蒸发得到NaCl晶体
B. 用10 mL的量筒量取4.8 mL的盐酸
C. 用托盘天平称取25.20 g NaCl
D. 用1000 mL容量瓶配制450 mL 0.1 mol·L-1的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,固定体积为2L密闭容器中,发生反应:
2SO2(g)+O2(g)![]() 2SO3(g ) ΔH <0,n(SO2)随时间的变化如表:
2SO3(g ) ΔH <0,n(SO2)随时间的变化如表:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
则下列说法正确的是
A. 当v(SO2)=v(SO3)时,说明该反应已达到平衡状态
B. 用O2表示0~4 min内该反应的平均速率为0.005 mol/(L·min)
C. 平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大
D. 若升高温度,则SO2的反应速率会变大,平衡常数K值会增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热条件下浓硫酸能将木炭粉氧化成CO2,本身被还原成SO2。试用如图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
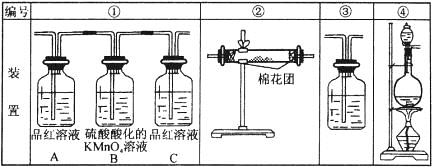
(1)这些装置的连接顺序是(按产物气流从左至右的方向,填写装置的编号):______→____→____→____。
(2)实验时可观察到装置①中A瓶的溶液褪色。A瓶溶液的作用是_________,B瓶溶液的作用是_______, C瓶溶液的作用是________________。写出B中发生的离子方程式__________。
(3)装置②中所加的固体药品是____________,可验证的产物是____________。
(4)装置③中所盛溶液是_____________,可验证的产物是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列科学成果中,由我国化学家在现代化学研究中取得的是( )
A.发现放射性元素钋和镭
B.现代量子化学的创立
C.人工全合成牛胰岛素
D.元素周期律的发现
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com