
2013年1月26日15时整,中国国产大型军用运输机运-20成功降落。标志着运-20首飞圆满成功。请回答下列问题:
Ⅰ.运-20根据结构和性能要求不同,使用的材料也不同,你认为下列材料中用于运-20制造,合理的是 (填序号)。
A.利用纯铝制造运-20发动机
B.用镁铝合金制造运-20座椅
C.用氧化铝制造运-20电器线路的导线
D.用普通钢制造运-20灭火器的外壳
Ⅱ.制造铝合金所需的铝从铝土矿中提取,已知铝土矿的主要成分为氧化铝(含有Fe2O3、SiO2杂质),SiO2不与盐酸反应但能溶解在NaOH溶液中生成可溶性Na2SiO3。工业上经过下列工艺可以冶炼金属铝:
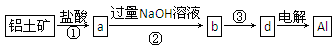
(1)①②中除加试剂外,还需要进行的操作是 。
(2)写出步骤②反应的化学方程式: 。
(3)③中需要通人过量的二氧化碳,写出该过程中含铝化合物发生反应的离子方程式: 。
(4)一种新型镁铝合金的化学式为Mg17Al12,科学家发现它具有储氢性能,是一种潜在的储氢材料,可在氩气保护下,将一定比例的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为Mg17Al12+17H2=17MgH2+12Al,得到的混合物Y(17MgH2+12Al)在一定条件下能释放出氢气。
①制备镁铝合金(Mg17Al12)时通人氩气的目的是 。
②在5.0 mol·L-1盐酸中,混合物Y能完全释放出H2。1 mol Mg17A112完全吸氢后得到的混合物Y与上述盐酸完全反应,消耗盐酸的体积为 L。
Ⅰ.BD
Ⅱ.(1)过滤
(2)AlCl3+4NaOH=NaAlO2+2H2O+3NaCl、FeCl3+3NaOH=Fe(OH)3↓+3NaCl
(3)AlO2-+CO2+H2O=Al(OH)3↓+HCO3-
(4)①防止Mg、Al与空气中的成分反应 ②14
【解析】Ⅰ.选项A,纯铝硬度差,不能用于制造飞机发动机。选项B,镁铝合金具有质量轻、密度低、散热性好、抗压性强和易于加工等性能,能用于制造运-20的座椅。选项C,固态氧化铝不导电,不能用于制造运-20电器线路的导线。选项D,普通钢制造的容器具有较好的抗压和抗冲击能力等特性,适合制造灭火器的外壳。
Ⅱ.(1)铝土矿中的Al2O3、Fe2O3能与盐酸反应生成可溶性AlCl3、FeCl3,SiO2不反应,a中含有固体SiO2,b中含有固体Fe(OH)3,均需要利用过滤除去。
(2)向AlCl3、FeCl3溶液中加入过量NaOH溶液,AlCl3、FeCl3与过量NaOH溶液反应生成可溶的NaAlO2和难溶的Fe(OH)3沉淀,据此可写出相应反应的化学方程式。
(3)NaAIO2溶液与过量CO2反应生成Al(OH)3沉淀和NaHCO3,其反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-。
(4)①由于Mg、Al都易在空气中燃烧,所以制备镁铝合金时通入氩气的目的是防止Mg、Al与空气中的成分反应。
②1 mol Mg17Al12完全吸氢后得到的混合物为17 mol MgH2和12 mol Al,与盐酸反应的化学方程式为MgH2+HCl=MgCl2+2H2↑、2Al+6HCl===2AlCl3+3H2↑,17 mol MgH2消耗34 mol HCl,12 mol Al消耗36 mol HCl,共消耗70 mol HCl,消耗5.0 mol·L-1盐酸的体积为70 mol÷5.0 mol·L-1=14 L。


科目:高中化学 来源:2014年高考化学苏教版总复习 1-4 氧化还原反应练习卷(解析版) 题型:选择题
氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:aHClO3=bO2↑+cCl2↑+dHClO4+eH2O,下列说法正确的是( )
A.由反应可知,氧气、氯气均为氧化产物
B.若化学计量数a=8,则该反应转移电子数为12e-
C.若b确定,则方程式中其他物质的化学计量数均能确定
D.若氯酸分解所得混合气体,1 mol混合气体质量为51.5 g,则反应方程式可表示为:5HClO3=O2↑+Cl2↑+3HClO4+H2O
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 1-2 物质的量、物质的聚集状态练习卷(解析版) 题型:选择题
下列说法中错误的是( )
A.从1 L 1 mol·L-1的NaCl溶液中取出10 mL,其浓度仍是1 mol·L-1
B.配制0.5 L 10 mol·L-1的盐酸,需要氯化氢气体112 L(标准状况)
C.0.5 L 2 mol·L-1 BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023
D.10 g 98%的硫酸(密度为1.84 g· cm-3)与10 mL 18.4 mol·L-1硫酸的浓度是不同的
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 1-1 物质的分类、转化及分散系练习卷(解析版) 题型:选择题
下列关于有关物质的叙述正确的是 ( )
①酸性氧化物肯定是非金属氧化物
②不能跟酸反应的氧化物一定能跟碱反应
③碱性氧化物肯定是金属氧化物
④分散系一定是混合物
⑤浊液均可用过滤的方法分离
A.①③ B.③④ C.②④ D.④⑤
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习3-3铁、铜的获取及应用练习卷(解析版) 题型:选择题
用黄色的FeCl3溶液分别进行下列实验,解释或结论不正确的是 ( )。
选项实验现象解释或结论
A加入FeCl3固体溶液变成红褐色FeCl3的水解程度变大
B加入等体积水溶液颜色变浅c(Fe3+)变小
C加入足量Fe粉溶液颜色变成浅绿色2Fe3++Fe=3Fe2+
D将FeCl3溶液微热溶液变成红褐色水解反应ΔH>0
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习3-2从铝土矿到铝合金练习卷(解析版) 题型:选择题
3 g镁铝合金与100 mL稀硫酸恰好完全反应,将反应后的溶液加热蒸干,得到无水硫酸盐17.4 g,则原硫酸的物质的量浓度为 ( )。
A.1 mol·L-1 B.1.5 mol·L-1
C.2 mol·L-1 D.2.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习3-1钠、镁及其化合物练习卷(解析版) 题型:填空题
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:
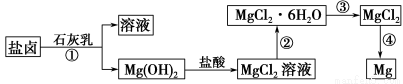
回答下列问题:
(1)工业上从盐卤中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是 。
(2)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是先将沉淀加入到盛有 溶液的烧杯中,充分搅拌后经 、 (填操作方法)可得纯净的Mg(OH)2。
(3)下图是该兴趣小组设计进行过程③的实验装置图:
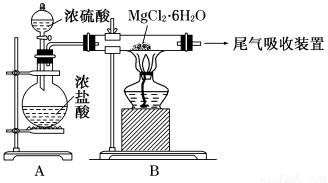
其中装置A的作用是 。
(4)写出过程④中发生反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习2-3-1氧化还原反应概念和规律练习卷(解析版) 题型:选择题
已知:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O,MnO2+4HCl MnCl2+Cl2↑+2H2O。其中KMnO4和一般浓度的盐酸即可反应,K2Cr2O7需和较浓盐酸(>6 mol·L-1)反应,MnO2需和浓盐酸(>8 mol·L-1)反应。根据以上信息,下列结论中不正确的是 ( )。
MnCl2+Cl2↑+2H2O。其中KMnO4和一般浓度的盐酸即可反应,K2Cr2O7需和较浓盐酸(>6 mol·L-1)反应,MnO2需和浓盐酸(>8 mol·L-1)反应。根据以上信息,下列结论中不正确的是 ( )。
A.上述反应均属于氧化还原反应
B.生成1 mol Cl2时,三个反应中转移的电子数相等
C.盐酸浓度越大,Cl-的还原性越强
D.氧化性:KMnO4>K2Cr2O7>Cl2>MnO2
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习1-2-1物质的量 气体摩尔体积练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列各项叙述中正确的有( )。
①0.2 mol H2O2完全分解转移的电子数为0.4NA
②25 ℃、101 kPa下,16 g O3和O2混合气体中含有的氧原子数为NA
③将含0.1 mol FeCl3的饱和溶液滴入沸水形成的胶体粒子的数目为0.1NA
④1 mol N2和3 mol H2在一定条件下的密闭容器中充分反应,容器内的分子数大于2NA
A.①②③ B.①②④ C.①②③④ D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com