
室温下,用0.10mol/L的盐酸滴定20.00mL 0.10mol/L的某碱BOH溶液得到的滴定曲线如下,下列判断不正确的是( )
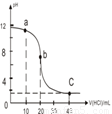
A.a点时,溶液呈碱性,溶液中c(B+)>c(Cl-)
B.b点时溶液的pH=7
C.当c(Cl-)=c(B+)时,V(HCl)<20mL
D.C点时溶液中c(H+)约为0.03mol/L
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 室温下,用0.10mol?L-1KOH溶液滴定10.00mL 0.10mol?L-1H2C2O4溶液所得的滴定曲线如图所示(混合溶液的体积可看成混合前两溶液的体积之和).请回答下列问题:
室温下,用0.10mol?L-1KOH溶液滴定10.00mL 0.10mol?L-1H2C2O4溶液所得的滴定曲线如图所示(混合溶液的体积可看成混合前两溶液的体积之和).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 (2011?崇川区三模)在室温下,用0.10mol?L-1 KOH溶液滴定10.00mL 0.10mol?L-1H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前两种溶液的体积之和).下列说法正确的是( )
(2011?崇川区三模)在室温下,用0.10mol?L-1 KOH溶液滴定10.00mL 0.10mol?L-1H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前两种溶液的体积之和).下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
| A、与AlCl3溶液发生反应的离子方程式为Al3++3OH-═Al(OH)3↓ | B、加水稀释后,溶液中c(NH4+)?c(OH-)变大 | C、用HNO3溶液完全中和后,溶液不显中性 | D、其溶液的pH=13 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com