��1����һ�ڿ����б�¶����KOH���壬������֪�京ˮ2.8%����K
2CO
337.3%������ΪKOH����ȡ1g��Ʒ���뵽25mL 2mol?L
-1������������������1.0mol?L
-1 KOH��Һ33.9mLǡ����ȫ�кͣ������кͺ���Һ�ɵõ�����
g������������ȷ��С�����3λ��
��2�������������������15g�У�����ϡ����150mL���ܷų�H
2 1.68L����״������ͬʱ��������������ʣ�࣬��Ӧ�����Һ�е���KSCN��Һ��δ����ɫ�仯��Ϊ���к�����H
2SO
4����ʹFe
2+��ȫת����Fe��OH��
2��������3mol?L
-1��NaOH��Һ200mL����ԭ��������ʵ���Ũ����
mol/L
��3��V L Fe
2��SO
4��
3��Һ�к���a g
��ȡ����Һ0.5V L����ˮϡ����2V L����ϡ�ͺ���Һ�� Fe
3+�����ʵ�����Ũ��Ϊ
mol/L ���������������ʽ��
��4��������ѧ�ҽ�Ǧ�������Ԫ�ص�ԭ�Ӻ˶�ײ�������һ��������Ϊ118��������Ϊ293����Ԫ�أ���ԭ��ԭ�Ӻ����������ͺ��������֮��Ϊ
��
��5���ڻ�ѧ��ӦaZn+bHNO
3��ϡ���TcZn��NO
3��
2+dNO��+eH
2O�У���e��ֵΪ4����d��ֵΪ
��




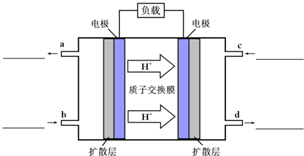 �״�-����ȼ�ϵ�أ�DMFC����һ�ָ�Ч�ܡ�����Ⱦ�綯�����ij��ص�أ���ȼ�ϵ�صĵ�ط�ӦʽΪ��CH3OH��l��+
�״�-����ȼ�ϵ�أ�DMFC����һ�ָ�Ч�ܡ�����Ⱦ�綯�����ij��ص�أ���ȼ�ϵ�صĵ�ط�ӦʽΪ��CH3OH��l��+
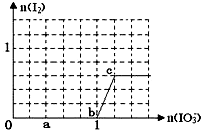 ��֪��Һ�У���ԭ��HSO3-��I-��������IO3-��I2��SO42-���ں�3molNaHSO3����Һ����μ���KIO3��Һ�������KIO3��������I2�����ʵ����Ĺ�ϵ��������ͼ��ʾ���Իش��������⣺
��֪��Һ�У���ԭ��HSO3-��I-��������IO3-��I2��SO42-���ں�3molNaHSO3����Һ����μ���KIO3��Һ�������KIO3��������I2�����ʵ����Ĺ�ϵ��������ͼ��ʾ���Իش��������⣺