联合国气候变化大会2009年12月7日在丹麦首都哥本哈根拉开帷幕,降低大气中CO
2的含量及有效地开发利用CO
2,引起了各国的普遍重视.
(1)工业上有一种方法是用CO
2来生产燃料甲醇.298.15K时,CO
2、H
2、与CH
3OH、H
2O的平均能量与合成甲醇反应的活化能的曲线图如图所示,据图回答问题:

①写出合成甲醇反应的热化学方程式
CO
2(g)+3H
2(g)

CH
3OH(g)+H
2O(g)△H=-(n-m)kJ?mol
-1CO
2(g)+3H
2(g)

CH
3OH(g)+H
2O(g)△H=-(n-m)kJ?mol
-1;
②在图中曲线
b
b
(填“a”或“b”)表示加入催化剂的能量变化曲线,催化剂能加快反应速率的原理是
催化剂能降低该反应的活化能,提高活化分子的百分数,化学反应速率加快
催化剂能降低该反应的活化能,提高活化分子的百分数,化学反应速率加快
;
③在体积为l L的密闭容器中,充入lmol CO
2和3mol H
2,测得CO
2和CH
3OH(g)的浓度随时间变化如图所示.

从反应开始到平衡,甲醇的平均反应速率v(CH
3OH)=
0.075mol?L-1?min-1
0.075mol?L-1?min-1
;
该反应的平衡常数k=
.
(2)乙醇是重要的化工产品和液体燃料,同样可以利用CO
2反应制取乙醇:
2CO
2(g)+6H
2(g)

CH
3CH
2OH(g)+3H
2O(g) 25℃时,K=2.95×10
11在一定压强下,测得反应的实验数据如下表.分析表中数据回答下列问题:
 |
500 |
600 |
700 |
800 |
| 1.5 |
45 |
33 |
20 |
12 |
| 2.0 |
60 |
43 |
28 |
15 |
| 3.0 |
83 |
62 |
37 |
22 |

①温度升高,K值
减小
减小
(填“增大”、“减小”、或“不变”).
②提高氢碳比[n(H
2)/n(CO
2)],K值
不变
不变
(填“增大”、“减小”、或“不变”),对生成乙醇
有利
有利
(填“有利”或“不利”).
③在右图的坐标系中作图说明压强变化对反应①的化学平衡的影响.并对图中横坐标、纵坐标的含义作必要的标注.


 CH3OH(g)+H2O(g)△H=-(n-m)kJ?mol-1
CH3OH(g)+H2O(g)△H=-(n-m)kJ?mol-1 CH3OH(g)+H2O(g)△H=-(n-m)kJ?mol-1
CH3OH(g)+H2O(g)△H=-(n-m)kJ?mol-1
 CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95×1011
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95×1011
 ①温度升高,K值
①温度升高,K值 CH3OH(g)+H2O(g)△H=-(n-m) kJ?mol-1,故答案为:CO2(g)+3H2(g)
CH3OH(g)+H2O(g)△H=-(n-m) kJ?mol-1,故答案为:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)△H=-(n-m) kJ?mol-1;
CH3OH(g)+H2O(g)△H=-(n-m) kJ?mol-1; CH3OH(g)+H2O(g),
CH3OH(g)+H2O(g), 或
或 ,故答案为:
,故答案为: 或
或 .
.

 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案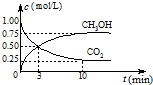
 CO+3H2
CO+3H2 CH3OH(g)+H2O(g)△H=-49.0kJ/mol,并达平衡.
CH3OH(g)+H2O(g)△H=-49.0kJ/mol,并达平衡.
