
如下图是实验室制备SO2并验证SO2某些性质的装置图 。试回答:
。试回答:
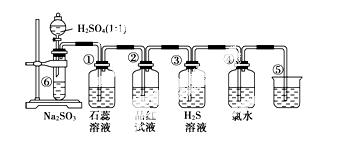
(1)⑥中发生的化学反应方程式为________________________________________________________________________。
(2)⑤的作用是________________________________,反应的离子方程式为__________________________。
(3)填表格
| 装置 | 实验现象 | 体现SO2的性质 |
| ① | ||
| ② | ||
| ③ | ||
| ④ |
 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
可逆反应mA(g)+nB(g)pC(g)+gD(g)的v-t图像如图甲所示,若其他条件都不变,只是
在反应前加入合适的催化剂,则其v-t图像如图乙所示。
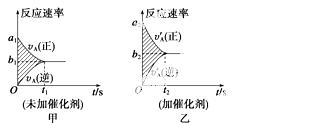
①a1=a2 ②a1<a2 ③b1=b2 ④b1<b2 ⑤t1>t2
⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧图Ⅱ中阴影部分面积更大
以上所列正确的为 ( )
A.②④⑤⑦ B.②④⑥⑧ C.②③⑤⑦ D.②③⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
将3.20 g Cu和10 mol·L-1的HNO3 30 mL充分反应,还原产物中有NO2和NO,若反应后溶液中有a mol H+,则此时溶液中NO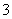 的物质的量为________ mol。
的物质的量为________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图小试管中盛有几毫升水,与大试管连通的U形细玻璃管内放有少量水(已染成红色)。如沿小试管壁慢慢注入3 mL浓硫酸,静置片刻后,U形细玻璃管中可观察到的现象是液面( )
A.左高右低 B.左低右高
C.左右一样高 D.来回振动
查看答案和解析>>
科目:高中化学 来源: 题型:
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图) ,下列说法正确的是( )
,下列说法正确的是( )
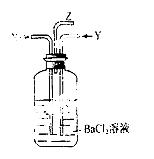 A.洗气瓶中产生的沉淀是
A.洗气瓶中产生的沉淀是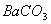
B.在Z导管出来的气体中无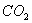
C.洗气瓶中产生的沉淀是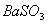
D.在Z导管口有红棕色气体出现
查看答案和解析>>
科目:高中化学 来源: 题型:
下列措施不合理的是
A.用SO2漂白纸浆和草帽辫
B.用硫酸清洗锅炉中的水垢
C.高温下用焦炭还原SiO2制取粗硅
D.用 Na2S作沉淀剂,除去废水中的Cu2+和Hg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)用化学方程式表示SO2形成硫酸型酸雨的反应:____________________。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是 。
(3)吸收液吸收SO2的过程中,pH随n(SO32-)∶n(HSO3-)变化关系如下表:
| n(SO32-)∶n(HSO3-) | 91∶9 | 1∶1 | 9∶91 |
| pH | 8.2 | 7.2 | 6.2 |
①由上表判断,NaHSO3溶液显 性,用化学平衡原理解释: 。
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母) 。
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
(4)当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下:

①HSO 3-在阳极放电的电极反应式是 。
3-在阳极放电的电极反应式是 。
②当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度压强下,在容积可变的密闭容器中发生反应 CO(g)+H2O(g)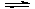 CO2(g)+H2(g)
CO2(g)+H2(g)
ΔH<0,则下列说法不正确的是
A.其他条件不变,加催化剂与不加催化剂其ΔH 相同
B.当达到平衡,向体系中充入CO2其平衡向左移动
C.理论上该反应可设计成燃料电池,H2O(g)在正极上发生还原反应
D.平衡混合气体通入NaOH溶液恰好反应,升高温度溶液碱性增强,其pH一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
重铬酸钠二水合物Na2Cr2O7·2H2O广泛用作氧化剂、金属表面精整、皮革制作等。以铬矿石(Cr2O3,含FeO、Al2O3、SiO2等杂质)为原料制取重铬酸钠的流程如下:

请回答下列问题:
(1)写出Cr2O3在高温焙烧生成Na2CrO4的化学方程式__________________________。
(2)调节pH后得到的沉淀主要是____________(填写化学式).
(3)写出用硫酸酸化使Na2CrO4转化为Na2Cr2O7的原理(写出离子方程式并加以文字说明):__________。
(4)氯化铬酸CrO2Cl2是红色液体,它可由Na2Cr2O7与NaCl的固体混合物和浓硫酸小心加热下制得,写出制备CrO2Cl2的化学反应方程式____________________________。
(5)某化工厂采用石墨作电极电解Na2CrO4溶液,实现Na2CrO4转化为Na2Cr2O7的生产,其原理如图所示。
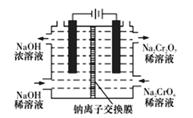
①通电后阳极区溶液的颜色变化为__________________________________。
②写出电解Na2CrO4溶液制备Na2Cr2O7的化学反应方程式:_______________________________。
③在电流为I A.通电时间为t s后,两极共收集到3.36 L气体(标准状况下),则阿伏加德罗常数的表达式NA =_____mol-1(己知电子的电量为1.6* 10-19C)。
(6)Na2Cr2O7可用于测定废水的化学耗氧量(即COD,指每升水样中还原性物质被氧化所需要的O2的质量,单位:mg·L-1),现有某水样200.00 mL,酸化后加入c1 mol/L的Na2Cr2O7溶液V1 mL,使水中的还原性物质完全被氧化(还原产物为Cr3+ );再用c2 mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2 mL。则该水样的COD为_____________mg·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com