


���� B�����Ӿ۷�Ӧ���ɾ�����ϩ����BΪCH2=CHCl����Ȳ��HCl����ȡ����Ӧ����B����Ȳ��ˮ�����ӳɷ�Ӧ������ȩ����ȩ��һ������������Ӧ����DΪCH3COOH��C��D��Ӧ����E��Ӧ��������Ӧ����E����������C���ڴ�������Ȳ�����������ӳɷ�Ӧ����AΪCH2=CH2����ϩ��ˮ�����ӳɷ�Ӧ����CΪCH3CH2OH���Ҵ������ᷢ��������Ӧ����EΪCH3COOCH2CH3���Դ������
��� �⣺��1��C�Ľṹ��ʽΪCH3CH2OH��������Ϊ�ǻ����ʴ�Ϊ���ǻ���
��2����Ӧ�ڵĻ�ѧ����ʽΪCH��CH+HCl$��_{��}^{����}$CH2=CHCl��������Ϊ˫����Ϊ�ӳɷ�Ӧ��
�ʴ�Ϊ��CH��CH+HCl$��_{��}^{����}$CH2=CHCl���ӳɷ�Ӧ��
��3����X�����ʽ������C2H2����ͬ��X��������������ܶ�Ϊ39������Է�������Ϊ39��2=78��$\frac{78}{13}$=6����֪XΪ����
A����ʵ��1��֪��X������ˮ�����ܶȱ�ˮС������ȡ�����ˮ�ֲ㣬ˮ���²㣬��A��ȷ��
B��ú̿�в������������������Ʒ������������B����
C��Xʹ��ˮ��ɫ��������ȡ��Ϊ�����仯����C����
D��ˮ���ټ�ˮ���ֲ㣬�л����ˮ����ˮ�ֲ㣬��������Թ�2�е��л������ϲ㻹���²㣬��ͨ����ˮȷ������D��ȷ��
�ʴ�Ϊ��AD��
���� ���⿼���л�����ƶϣ�Ϊ��Ƶ���㣬�����л�������ʡ��л���Ӧ�ƶ��л���Ϊ���Ĺؼ������ط������ƶ������Ŀ��飬ע�ⳣ���л�������ʼ�Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ������Ϊ���淴ӦA��g��+2B��g��?2C��g�� ����ӦΪ���ȷ�Ӧ��ƽ���ƶ���ϵ���ߣ�����˵����ȷ���ǣ�������
��ͼ������Ϊ���淴ӦA��g��+2B��g��?2C��g�� ����ӦΪ���ȷ�Ӧ��ƽ���ƶ���ϵ���ߣ�����˵����ȷ���ǣ�������| A�� | a��b��y��ָB���������� | B�� | a��b��y��ָC���������� | ||
| C�� | a��b��y��ָA��ת���� | D�� | a��b��y��ָA��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.9g | B�� | 4.5g | C�� | 9.0mol | D�� | 13.5mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
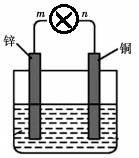 ��������Ϊ100g��пƬ��ͭƬ�õ�������ݴ�������ʢ��500mL 2mol•L-1ϡ������Һ��1.5L�����й�����ͼװ�ã�
��������Ϊ100g��пƬ��ͭƬ�õ�������ݴ�������ʢ��500mL 2mol•L-1ϡ������Һ��1.5L�����й�����ͼװ�ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 �� D�����й����ŵ��������Ȼ���
�� D�����й����ŵ��������Ȼ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ʒ�ȸ�����Ʒ����ʴ | |
| B�� | ͬ�ֽ�����Ϊԭ��ص���������Ϊ���ص�������ʴ�ø��� | |
| C�� | �ֹܶ�пʱ��п�����������ֹ���������п����Һ���������Һ | |
| D�� | ��Ƭ�������ⷽ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | Ŀ�� | ���뷽�� | ԭ�� |
| A | ��������ˮ�ĵ� | ����ȡ | �����ܶȱ�ˮС |
| B | ���������������Ҵ� | ��Һ | �����������Ҵ����ܶȲ�ͬ |
| C | ��ȥKNO3�����л��ӵ�NaCl | �ؽᾧ | KNO3��ˮ�е��ܽ�Ⱥܴ� |
| D | ��ȥ�����е�̼����� | ���� | ���ȶ���ͬ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʧ����������Na��K | B�� | ���ԣ�NaOH��KOH | ||
| C�� | �õ���������S��Cl | D�� | ���ԣ�HClO4��H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO��g��+O2��g��?2NO2��g����ϵ�У�c��NO����ʱ��ı仯�����
��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO��g��+O2��g��?2NO2��g����ϵ�У�c��NO����ʱ��ı仯�����| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| c��NO����mol/L�� | 0.10 | 0.05 | 0.04 | 0.03 | 0.03 | 0.03 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com