
【题目】工业上以铬铁矿(主要成分为FeOCr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O72H2O),其主要反应为: ①4FeOCr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
②2Na2CrO4+H2SO4Na2SO4+Na2Cr2O7+H2O
下列说法中正确的是( )
A.反应①和②均为氧化还原反应
B.反应①的氧化剂是O2 , 还原剂是FeOCr2O3
C.高温下,O2的氧化性大于Fe2O3小于Na2CrO4
D.生成1mol的Na2Cr2O7时共转移5mol电子
【答案】B
【解析】解:A、4FeOCr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2中有元素化合价的变化,所以是氧化还原反应,而2Na2CrO4+H2SO4
8Na2CrO4+2Fe2O3+8CO2中有元素化合价的变化,所以是氧化还原反应,而2Na2CrO4+H2SO4 ![]() Na2SO4+Na2Cr2O7+H2O中没有元素化合价的变化,所以不是氧化还原反应,故A错误; B、4FeOCr2O3+8Na2CO3+7O2
Na2SO4+Na2Cr2O7+H2O中没有元素化合价的变化,所以不是氧化还原反应,故A错误; B、4FeOCr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2中,氧气中氧元素得电子化合价降低,所以氧化剂是氧气,铁元素和铬元素失电子化合价升高,所以还原剂是FeOCr2O3 , 故B正确;
8Na2CrO4+2Fe2O3+8CO2中,氧气中氧元素得电子化合价降低,所以氧化剂是氧气,铁元素和铬元素失电子化合价升高,所以还原剂是FeOCr2O3 , 故B正确;
C、4FeOCr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2中,氧化剂是氧气,还原剂是FeOCr2O3 , 所以氧气的氧化性大于Na2CrO4和Fe2O3 , 但不能判断Na2CrO4和Fe2O3的氧化性相对强弱,故C错误;
8Na2CrO4+2Fe2O3+8CO2中,氧化剂是氧气,还原剂是FeOCr2O3 , 所以氧气的氧化性大于Na2CrO4和Fe2O3 , 但不能判断Na2CrO4和Fe2O3的氧化性相对强弱,故C错误;
D、由方程式4FeOCr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2转移电子可知,生成1molNa2CrO4时,参加反应的O2的物质的量为
8Na2CrO4+2Fe2O3+8CO2转移电子可知,生成1molNa2CrO4时,参加反应的O2的物质的量为 ![]() mol,反应中O元素由0价降低为﹣2价,电子转移的物质的量为参加反应的氧气的物质的量的4倍,转移电子的物质的量为
mol,反应中O元素由0价降低为﹣2价,电子转移的物质的量为参加反应的氧气的物质的量的4倍,转移电子的物质的量为 ![]() mol×4=3.5mol,所以反应①中每生成1molNa2CrO4时电子转移3.5mol,反应②不是氧化还原反应,所以生成1mol的Na2Cr2O7时转移7mol电子,故D错误;
mol×4=3.5mol,所以反应①中每生成1molNa2CrO4时电子转移3.5mol,反应②不是氧化还原反应,所以生成1mol的Na2Cr2O7时转移7mol电子,故D错误;
故选B.


科目:高中化学 来源: 题型:
【题目】常温下,将0.1molL﹣1CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起( )
A.溶液的pH增加 B.CH3COOH电离度变大
C.溶液的导电能力减弱 D.溶液中c(OH﹣)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铝及其化合物的叙述正确的是( )
A.Al是地壳中含量最多的元素
B.Al2O3的熔点很高,是一种较好的耐火材料
C.向Al2(SO4)3溶液中滴加过量NaOH溶液制备Al(OH) 3
D.铝制品在生活中被广泛使用,说明铝是一种不活泼的金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将过量过氧化钠投入到氯化亚铁溶液中,可观察到的现象是
A. 只有气泡产生 B. 生成灰绿色沉淀
C. 生成白色沉淀 D. 生成红褐色沉淀并有气泡产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.1 mol NH4+ 所含质子数为10NA
B.10克氖气所含原子数约为6.02×1023
C.标准状况下,22.4 L SO2所含的分子数为NA
D.常温常压下,32 g O2和O3的混合气体所含原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼与铝的性质相似,能与氧气、氢氧化钠溶液等物质反应.硼与氯气反应生成三氯化硼(BCl3),生成的三氯化硼遇水水解产生白雾(BCl3+3H2O=H3BO3+3HCl)(已知:BCl3的熔点为﹣107.3℃,沸点为12.5℃),且三氯化硼用于制取乙硼烷(B2H6).某兴趣小组设计如图所示装置制备三氯化硼. 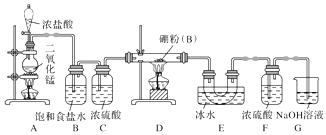
回答下列问题:
(1)盛浓盐酸的装置名称为 .
(2)装置E的作用是
(3)装置D中发生反应的化学方程式为 .
(4)装置F的作用是 , 可以用一个盛装(填试剂名称)的干燥管代替装置F和G,使实验更简便.
(5)为了顺利完成实验,点燃酒精灯的正确操作是(填字母),其理由是 . a.先点燃A处酒精灯,后点燃D处酒精灯
b.先点燃D处酒精灯,后点燃A处酒精灯
c.同时点燃A、D两处酒精灯.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.在一定体积和一定条件下有反应N2(g)+3H2(g)![]() 2NH3(g),现分别从两条途径建立平衡:
2NH3(g),现分别从两条途径建立平衡:
Ⅰ.起始浓度N2:1 mol·L-1,H2:3 mol·L-1
Ⅱ.起始浓度N2:2 mol·L-1,H2:6 mol·L-1
则下列叙述正确的是( )
A. Ⅰ和Ⅱ两途径达到平衡时,体系内各成分的体积分数相同
B. 达到平衡时,途径Ⅰ的反应速率v(H2)等于途径Ⅱ的反应速率v(H2)
C. 达到平衡时,途径Ⅱ体系内混合气体的压强是途径Ⅰ内混合气体压强的2倍
D. 达到平衡时,途径Ⅰ体系内混合气体的密度为途径Ⅱ体系内混合气体的密度的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】张青莲是我国著名的化学家,1991年他准确测得In的相对原子质量为114.818,被国际相对原子质量委员会采用为新的标准值.这是相对原子质量表中首次采用我国测定的相对原子质量值.则下列关于 ![]() In的说法中,错误的是( )
In的说法中,错误的是( )
A.![]() In原子核外有49个电子
In原子核外有49个电子
B.![]() In原子核内有49个中子
In原子核内有49个中子
C.![]() In原子核内质子数和中子数之和等于其质量数,为115
In原子核内质子数和中子数之和等于其质量数,为115
D.![]() In是In元素的一种核素
In是In元素的一种核素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com