
 ŌĖÓĆĖłŃ§»ÆѧŌĄķ£¬½ā¾öĻĀĮŠĪŹĢā£ŗ
ŌĖÓĆĖłŃ§»ÆѧŌĄķ£¬½ā¾öĻĀĮŠĪŹĢā£ŗ| ĪĀ¶Č/ | 400 | 500 | 800 |
| Ę½ŗā³£ŹżK | 9.94 | 9 | 1 |
·ÖĪö £Ø1£©“¦Ąķŗ¬CN-·ĻĖ®Ź±£¬ÓĆNaOHČÜŅŗµ÷½ŚÖĮpH=9Ź±£Ø³£ĪĀ£©£¬Ka£ØHCN£©=6.17”Į10-10£¬Kh=$\frac{c£ØO{H}^{-}£©c£ØHCN£©}{c£ØC{N}^{-}£©}$”Į$\frac{c£Ø{H}^{+}£©}{c£Ø{H}^{+}£©}$=$\frac{Kw}{Ka}$=1.6”Į10-5£¬c£ØOH-£©=10-5£¬Ōņ$\frac{c£ØHCN£©”Į1{0}^{-5}}{c£ØC{N}^{-}£©}$=1.6”Į10-5£»
£Ø2£©ÓÉøĒĖ¹¶ØĀɼĘĖć£¬¢Ł+¢Ś-¢ŪµĆµ½¹¤ŅµÉĻÉś²ś“Ö¹čµÄČČ»Æѧ·½³ĢŹ½£»
£Ø3£©Ķ¼±ķ·ÖĪöæÉÖŖ£¬ĖęĪĀ¶ČÉżøߣ¬Ę½ŗā³£Źż¼õŠ”£¬ĖµĆ÷Ę½ŗāÄęĻņ½ųŠŠ£¬Õż·“Ó¦ĪŖ·ÅČČ·“Ó¦£»½įŗĻ»ÆŃ§Ę½ŗāČż¶ĪŹ½ĮŠŹ½¼ĘĖćŅ»Ńõ»ÆĢ¼µÄ×Ŗ»ÆĀŹ£»
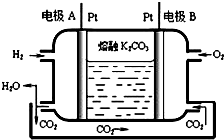
£Ø4£©×°ÖĆĶ¼æÉÖŖĶØČėĒāĘųµÄµē¼«ĪŖŌµē³Ųøŗ¼«Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬ŌŚČŪČŚK2CO3ÖŠÉś³É¶žŃõ»ÆĢ¼£¬½įŗĻµē×ÓŹŲŗćŗĶµēŗÉŹŲŗćŹéŠ“µē¼«·“Ó¦£®
½ā“š ½ā£ŗ£Ø1£©“¦Ąķŗ¬CN-·ĻĖ®Ź±£¬ÓĆNaOHČÜŅŗµ÷½ŚÖĮpH=9Ź±£Ø³£ĪĀ£©£¬CN-+H2O?HCN+OH-£¬Ka£ØHCN£©=6.17”Į10-10£¬Kh=$\frac{c£ØO{H}^{-}£©c£ØHCN£©}{c£ØC{N}^{-}£©}$”Į$\frac{c£Ø{H}^{+}£©}{c£Ø{H}^{+}£©}$=$\frac{Kw}{Ka}$=$\frac{1{0}^{-14}}{6.17”Į1{0}^{-10}}$=1.6”Į10-5£¬c£ØOH-£©=10-5£¬Ōņ$\frac{c£ØHCN£©”Į1{0}^{-5}}{c£ØC{N}^{-}£©}$=1.6”Į10-5£¬Ōņc£ØCN-£©£¼c£ØHCN£©£»
¹Ź“š°øĪŖ£ŗ£¼£»
£Ø2£©¢ŁC£Øs£©+O2£Øg£©ØTCO2£Øg£©£»”÷H=a kJ•mol-1£»
¢ŚCO2£Øg£©+C£Øs£©ØT2CO£Øg£©£»”÷H=b kJ•mol-1£»
¢ŪSi£Øs£©+O2£Øg£©ØTSiO2£Øs£©£»”÷H=c kJ•mol-1£®
ÓÉøĒĖ¹¶ØĀÉæÉÖŖ£¬¢Ł+¢Ś-¢ŪµĆµ½¹¤ŅµÉĻÉś²ś“Ö¹čµÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ2C£Øs£©+SiO2£Øs£©ØTSi£Øs£©+2CO£Øg£©”÷H=£Øa+b-c£©kJ•mol-1£»
¹Ź“š°øĪŖ£ŗ2C£Øs£©+SiO2£Øs£©ØTSi£Øs£©+2CO£Øg£©”÷H=£Øa+b-c£©kJ•mol-1£»
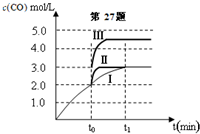
£Ø3£©Ķ¼±ķŹż¾Ż·ÖĪöæÉÖŖ£¬ĖęĪĀ¶ČÉżøߣ¬Ę½ŗā³£Źż¼õŠ”£¬ĖµĆ÷Ę½ŗāÄęĻņ½ųŠŠ£¬Õż·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ģŹ±äĪŖøŗÖµ£»
500”ꏱ½ųŠŠøĆ·“Ó¦£¬ĒŅCOŗĶH2OĘšŹ¼ÅضČĻąµČÉčĪŖx£¬Ņ»Ńõ»ÆĢ¼ĻūŗÄĪļÖŹµÄĮæĪŖy£¬Ōņ
CO£Øg£©+H2O£Øg£©?H2£Øg£©+CO2£Øg£©£®
ĘšŹ¼Įæ£Ømol£© x x 0 0
±ä»ÆĮæ£Ømol£© y y y y
Ę½ŗāĮæ£Ømol£© x-y x-y y y
K=$\frac{{y}^{2}}{£Øx-y£©^{2}}$=9
$\frac{y}{x-y}$=3£¬3x=4y
COĘ½ŗā×Ŗ»ÆĀŹ=$\frac{y}{x}$”Į100%=$\frac{3}{4}$”Į100%=75%£»
¹Ź“š°øĪŖ£ŗ£¼£»75%£»
£Ø4£©×°ÖĆĶ¼ÖŠĶØČėĒāĘųµÄµē¼«ĪŖŌµē³Ųøŗ¼«Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬ŌŚČŪČŚK2CO3ÖŠÉś³É¶žŃõ»ÆĢ¼£¬½įŗĻµē×ÓŹŲŗćŗĶµēŗÉŹŲŗćæÉÖŖµē¼«·“Ó¦ĪŖH2-2e-+CO32-ØTCO2+H2O£¬
¹Ź“š°øĪŖ£ŗH2-2e-+CO32-ØTCO2+H2O£®
µćĘĄ ±¾Ģāæ¼²éĮĖČČ»Æѧ·½³ĢŹ½ŹéŠ“£¬Ōµē³Ųµē½ā³ŲŌĄķµÄ·ÖĪöÅŠ¶Ļ£¬»ÆŃ§Ę½ŗā¼ĘĖćÓ¦ÓĆ£¬ÕĘĪÕ»ł“”ŹĒ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH2OÓėC2H4O2 | B£® | C4H10ÓėC4H6O | C£® | CF2Cl2ÓėC2F2Cl2 | D£® | C4H10ÓėC3H6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| ĪļÖŹ | ŠŌÖŹ£Ø·Šµć¼°·Ö½āĪĀ¶Č¾łĪŖ101kPa²āµĆ£© |
| ĮŚ±½¶ž¼×Ėįōū £ØM=148g/mol£© | °×É«Õėד¾§Ģ壮²»ČÜÓŚĄäĖ®£¬ČÜÓŚČČĖ®¼°ÓŠ»śČܼĮ£® ĆܶČ1.53g/cm3£¬·Šµć295”ę£® |
| Õż¶”“¼£ØM=74g/mol£© | ĪŽÉ«ŅŗĢ壮Ī¢ČÜÓŚĖ®£¬ČÜÓŚÓŠ»śČܼĮ£®ĆܶČ0.81g/cm3£¬·Šµć117.7”ę£®æÉÓėĖ®ŠĪ³É¶žŌŖ¹²·ŠĪļ£Ø·Šµć92.7”ę£©£® |
| ĮŚ±½¶ž¼×Ėį¶ž¶”õ„ £ØM=278g/mol£© | ĪŽÉ«ÓĶדŅŗĢ壮ÄŃČÜÓŚĖ®£¬ČÜÓŚÓŠ»śČܼĮ£®ĆܶČ1.49g/cm3£¬·Šµć340”ę£®ĖįŠŌĢõ¼žĻĀ180”ęŅŌÉĻŅ×·¢Éś·Ö½ā£® |
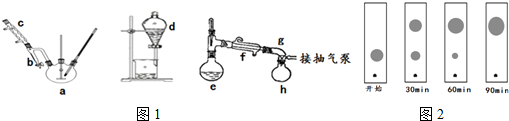
 ×Ŗ±ä³ÉŃĪ£¬“Ó¶ųÓė²śĪļ·ÖĄė£¬øĆ²Ł×÷ŹĒ·ńæÉøÄÓĆNaOHČÜŅŗ£æ·ń£ØĢī”°ŹĒ”±»ņ”°·ń”±£©£¬ŌŅņŹĒ£»ĒāŃõ»ÆÄĘ¼īŠŌĢ«Ē棬ÄÜŹ¹ĮŚ±½¶ž¼×Ėį¶ž¶”õ„·¢ÉśĖ®½ā£»£®¼ÓČėŹ³ŃĪĖ®Ļ“µÓŅ»·½ĆęŹĒ·ĄÖ¹ÓŠ»śĪļ·¢ÉśČé»Æ¶ų²»ĄūÓŚ·Ö²ć£¬ĮķŅ»·½ĆęŹĒĪŖĮĖ½µµĶĮŚ±½¶ž¼×Ėį¶ž¶”õ„µÄČܽā¶Č£®
×Ŗ±ä³ÉŃĪ£¬“Ó¶ųÓė²śĪļ·ÖĄė£¬øĆ²Ł×÷ŹĒ·ńæÉøÄÓĆNaOHČÜŅŗ£æ·ń£ØĢī”°ŹĒ”±»ņ”°·ń”±£©£¬ŌŅņŹĒ£»ĒāŃõ»ÆÄĘ¼īŠŌĢ«Ē棬ÄÜŹ¹ĮŚ±½¶ž¼×Ėį¶ž¶”õ„·¢ÉśĖ®½ā£»£®¼ÓČėŹ³ŃĪĖ®Ļ“µÓŅ»·½ĆęŹĒ·ĄÖ¹ÓŠ»śĪļ·¢ÉśČé»Æ¶ų²»ĄūÓŚ·Ö²ć£¬ĮķŅ»·½ĆęŹĒĪŖĮĖ½µµĶĮŚ±½¶ž¼×Ėį¶ž¶”õ„µÄČܽā¶Č£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

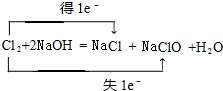 £»
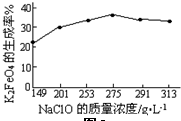
£»
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
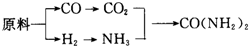
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ¼×“¼ŹĒÖŲŅŖµÄ»Æѧ¹¤Ņµ»ł“”ŌĮĻŗĶĒå½ąŅŗĢåČ¼ĮĻ£®¹¤ŅµÉĻæÉĄūÓĆCO»ņCO2Ą“Éś²śČ¼ĮĻ¼×“¼£®ŅŃÖŖ¼×“¼ÖʱøµÄÓŠ¹Ų»Æѧ·“Ó¦ŅŌ¼°ŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄ»Æѧ·“Ó¦Ę½ŗā³£ŹżČēĻĀ±ķĖłŹ¾£ŗ
¼×“¼ŹĒÖŲŅŖµÄ»Æѧ¹¤Ņµ»ł“”ŌĮĻŗĶĒå½ąŅŗĢåČ¼ĮĻ£®¹¤ŅµÉĻæÉĄūÓĆCO»ņCO2Ą“Éś²śČ¼ĮĻ¼×“¼£®ŅŃÖŖ¼×“¼ÖʱøµÄÓŠ¹Ų»Æѧ·“Ó¦ŅŌ¼°ŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄ»Æѧ·“Ó¦Ę½ŗā³£ŹżČēĻĀ±ķĖłŹ¾£ŗ| »Æѧ·“Ó¦ | Ę½ŗā³£Źż | ĪĀ¶Č”ę | |
| 500 | 800 | ||
| ¢Ł2H2£Øg£©+CO£Øg£©?CH3OH£Øg£© | K1 | 2.5 | 0.15 |
| ¢ŚH2£Øg£©+CO2£Øg£©?H2O £Øg£©+CO£Øg£© | K2 | 1.0 | 2.50 |
| ¢Ū3H2£Øg£©+CO2£Øg£©?CH3OH£Øg£©+H2O £Øg£© | K3 | ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ij½šŹōŌŖĖŲ“Ó»ÆŗĻĢ¬±äĪŖÓĪĄėĢ¬Ź±£¬øĆŌŖĖŲŅ»¶Ø·¢Éś»¹Ō·“Ó¦ | |
| B£® | ŗ¬½šŹōŌŖĖŲµÄĄė×Ó£¬Ņ»¶Ø¶¼ŹĒŃōĄė×Ó | |
| C£® | ½šŹōŃōĄė×Ó±»»¹ŌŅ»¶ØµĆµ½½šŹōµ„ÖŹ | |
| D£® | ŌŚŃõ»Æ»¹Ō·“Ó¦ÖŠ£¬½šŹōµ„ÖŹŅ»¶Ø±»»¹Ō |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
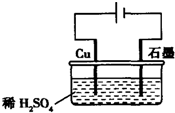
| A£® | µē½ā¹ż³ĢÖŠ£¬Ķµē¼«ÉĻÓŠH2²śÉś | |
| B£® | µē½ā³õĘŚ£¬Ö÷ŅŖ·“Ó¦·½³ĢŹ½ĪŖ£ŗCu+H2SO4$\frac{\underline{\;µē½ā\;}}{\;}$CuSO4+H2”ü | |
| C£® | µē½āŅ»¶ØŹ±¼äŗó£¬ŹÆÄ«µē¼«ÉĻÓŠĶĪö³ö | |
| D£® | Õūøöµē½ā¹ż³ĢÖŠ£¬H+µÄÅØ¶Č²»¶ĻŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ½ńÄźĮ½»įµÄŅ»øöÖ÷ĢāŹĒ»·¾³±£»¤£¬ÖĪĄķĪķö²ĢģĘųŹĒĪŅĆĒÄæĒ°×īÖ÷ŅŖµÄŅ»øöČĪĪń£®ČēĶ¼ŹĒ±±¾©Ķ³¼ĘµÄĪķö²ĢģĘųµÄĄ“Ō“ŗĶ³É·Ö·ÖĪö£ŗĻĀĮŠ¶ŌÓŚÖĪĄķĪķö²ĢģĘų“ėŹ©ĆčŹö²»ÕżČ·µÄŹĒ£Ø””””£©
½ńÄźĮ½»įµÄŅ»øöÖ÷ĢāŹĒ»·¾³±£»¤£¬ÖĪĄķĪķö²ĢģĘųŹĒĪŅĆĒÄæĒ°×īÖ÷ŅŖµÄŅ»øöČĪĪń£®ČēĶ¼ŹĒ±±¾©Ķ³¼ĘµÄĪķö²ĢģĘųµÄĄ“Ō“ŗĶ³É·Ö·ÖĪö£ŗĻĀĮŠ¶ŌÓŚÖĪĄķĪķö²ĢģĘų“ėŹ©ĆčŹö²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ³ä·ÖµÄĻ“µÓČ¼Ćŗ£¬³żČ„Č¼Ćŗ±ķĆęµÄ»Ņ³¾ | |
| B£® | ¼ÓæģĪŅ¹śÓÉ”°Č¼Ćŗ”±Ź±“ś½ųČėµ½”°ÓĶĘų”±Ź±“śµÄ²½·„ | |
| C£® | ²ÉÓĆ“ß»Æ×Ŗ»»¼¼Źõ½«Ęū³µĪ²ĘųÖŠµÄNO2ŗĶCO×Ŗ»ÆĪŖĪŽ¶¾ĘųĢå | |
| D£® | “¦ĄķNO2µÄŅ»ÖÖ·½·ØŹĒĄūÓĆ¼×Ķé“߻ƻ¹ŌNO2£¬ČōCH4£Øg£©+4NO2£Øg£©=4NO£Øg£©+CO2£Øg£©+2H2O£Øg£©£»”÷H=-512kJ•mol-1£¬Ōņ1g¼×Ķ铦ĄķNO2ŠčŅŖ·Å³ö16kJµÄČČĮæ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com