
| A. | ①②③⑤ | B. | ②③⑤⑥ | C. | ①④⑤⑥ | D. | ③④⑤⑥ |
分析 ①碳酸比盐酸弱,CO2与CaCl2溶液不会反应;
②酸性氧化物能与碱反应,过量的CO2与Ca(OH)2 反应生成Ca(HCO3)2;
③碳酸比硅酸强,过量的CO2与Na2SiO3溶液反应生成H2SiO3;
④过量的CO2通入饱和Na2CO3溶液中发生Na2CO3+H2O+CO2═2NaHCO3↓,因为碳酸氢钠溶解度比碳酸钠小;
⑤NaAlO2溶液通入过量的二氧化碳,由于碳酸酸性比氢氧化铝强,所以生成氢氧化铝白色沉淀和碳酸氢钠;
⑥通入CO2与NH3和NaCl反应生成氯化铵和碳酸氢钠.
解答 解:①碳酸比盐酸弱,CO2与CaCl2溶液不会反应,无沉淀生成,故①错误;
②酸性氧化物能与碱反应,过量的CO2与Ca(OH)2 反应:Ca(OH)2+2CO2═Ca(HCO3)2,无沉淀生成,故②错误;
③碳酸比硅酸强,过量的CO2与Na2SiO3溶液反应:2CO2+Na2SiO3+2H2O═2NaHCO3+H2SiO3↓,产生硅酸沉淀,故③正确;
④过量的CO2通入饱和Na2CO3溶液中发生反应:Na2CO3+H2O+CO2═2NaHCO3↓,因为碳酸氢钠溶解度比碳酸钠小,所以有NaHCO3晶体析出,故④正确;
⑤NaAlO2溶液通入过量的二氧化碳,由于碳酸酸性比氢氧化铝强,所以生成氢氧化铝白色沉淀和碳酸氢钠,2H2O+NaAlO2+CO2=Al(OH)3↓+NaHCO3,故⑤正确;
⑥通入CO2与NH3和NaCl反应生成氯化铵和碳酸氢钠,碳酸氢钠的溶解度较小,则最终析出碳酸氢钠晶体,故⑥正确;
故选D.
点评 本题考查物质的性质及反应,为高频考点,把握物质的性质、发生的反应及现象为解答的关键,侧重分析与应用能力的考查,注意⑥中碳酸氢钠的溶解度较小,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 质量相等时,三种气体所含原子数相等 | |
| B. | 质量相等时,三种气体所含氮原子数相等 | |
| C. | 所含氮原子数相等时,三种气体的质量相等 | |
| D. | 质量相等时,二氧化氮所含氧原子数比一氧化氮所含氧原子数多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鸡蛋清的水溶液加饱和(NH4)2SO4溶液后,有白色物质析出 | |
| B. | NO2气体经加压变成无色液体 | |
| C. | 溴水滴入植物油中振荡褪色 | |
| D. | 用SO2漂白的草帽日久变黄 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X原子的电子层数比Y原子的电子层数多 | |
| B. | X的氢化物的水溶液酸性比Y的氢化物的水溶液酸性强 | |
| C. | X的气态氢化物比Y的气态氢化物稳定 | |
| D. | Y的单质能将X从NaX的溶液中置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
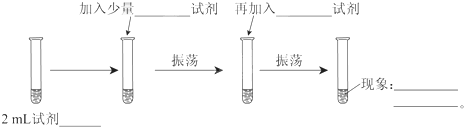
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
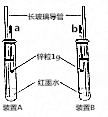 某化学兴趣小组按图示装好了实验装置,一支胶头滴管盛有盐酸,另一支胶头滴管盛有同体积、同浓度的醋酸.实验时同时完全捏扁a、b的胶头,观察实验现象.
某化学兴趣小组按图示装好了实验装置,一支胶头滴管盛有盐酸,另一支胶头滴管盛有同体积、同浓度的醋酸.实验时同时完全捏扁a、b的胶头,观察实验现象.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com