
����Ŀ��A��B��C��D��E���Ƕ���������Ԫ�أ���ԭ��������������A��Bͬ���ڣ�A��Dͬ���壬Aԭ���������������ڲ�������Ķ�����BԪ������������������������B����������C�������ӵ��Ӳ�ṹ��ͬ��C�ĵ�����B�ĵ����ڲ�ͬ�����·�Ӧ��������C2B��C2B2,E������������ԭ�Ӱ뾶��С��Ԫ�أ���ش�:
��1��D��Ԫ�����ڱ��е�λ����___________��
��2��C2B2�ĵ���ʽ��________
��3��B��C��E�����Ӱ뾶�ɴ�С��˳��Ϊ________(�����ӷ��Żش�); A��D��EԪ������������Ӧˮ�����������ǿ����Ϊ_________(�û�ѧʽ�ش���ͬ),B����̬�⻯����H2S��ȷе�ߵ���_____
��4��д��D��������������ᷴӦ�Ļ�ѧ����ʽ____________
��5��ˮ���̺�����������ʹ��ߺ�����Ⱦɫ��ʹˮ������ζ��EB2����������ȥˮ�г����Mn2+,���ɺ�ɫ����MnO2,������13.50g EB2ʱ����ת����lmol���ӣ���Ӧ�����ӷ���ʽ__________
���𰸡� �������ڵ�IVA�� ![]() Cl- ��O2-��Na+ HClO4��H2CO3��H2SiO3 H2O SiO2+4HF=SiF4��+2H2O 2ClO2+5Mn2++6H2O=5MnO2��+2Cl-+12H+
Cl- ��O2-��Na+ HClO4��H2CO3��H2SiO3 H2O SiO2+4HF=SiF4��+2H2O 2ClO2+5Mn2++6H2O=5MnO2��+2Cl-+12H+
��������A��B��C��D��E���Ƕ�����Ԫ�أ���ԭ��������������Aԭ���������������ڲ�������Ķ�������AΪ̼Ԫ�أ�A��Dͬ�壬��DΪ��Ԫ�أ�A��Bͬ���ڣ�BԪ��������������������������BΪ��Ԫ�أ�B����������C�������ӵ��Ӳ�ṹ��ͬ��C�ĵ����� B �ĵ����ڲ�ͬ�����·�Ӧ��������C2B��C2B2����CΪ��Ԫ�أ�E������������ԭ�Ӱ뾶��С��Ԫ�أ���EΪ��Ԫ�أ�����
��1��DΪ��Ԫ�أ���Ԫ�����ڱ��е������ڵڢ�A�壻��2��C2B2��Na2O2�������ʽ�ǣ�![]() ����3�����Ӳ���Խ�࣬���Ӱ뾶Խ���Ӳ�����ͬʱ���˵����Խ�࣬���Ӱ뾶ԽС������B��C��E���Ӱ뾶���ɴ�С��˳��Ϊr(Cl��)>r(O2��)>r(Na+)��Ԫ�صķǽ�����Խǿ����Ӧ������������Ӧˮ��������Ծ�Խǿ���ǽ�����Cl��C��Si����������HClO4��H2CO3��H2SiO3������ˮ����֮�����������Ǽ��Է��ӣ�����ˮ�ķе����H2S����4��д��D��������SiO2������ᷴӦ����SiF4��ˮ����Ӧ�Ļ�ѧ����ʽΪ��SiO2+4HF=SiF4��+2H2O����5����ClO2������Mn2+�����ɺ�ɫ����MnO2��������13.50g ����0.2mol��ClO2ʱ����ת����1mol���ӣ����ݵ��ӵ�ʧ�غ��д����Ӧ�����ӷ���ʽΪ5Mn2++2ClO2+6H2O=2Cl��+5MnO2��+12H+��
����3�����Ӳ���Խ�࣬���Ӱ뾶Խ���Ӳ�����ͬʱ���˵����Խ�࣬���Ӱ뾶ԽС������B��C��E���Ӱ뾶���ɴ�С��˳��Ϊr(Cl��)>r(O2��)>r(Na+)��Ԫ�صķǽ�����Խǿ����Ӧ������������Ӧˮ��������Ծ�Խǿ���ǽ�����Cl��C��Si����������HClO4��H2CO3��H2SiO3������ˮ����֮�����������Ǽ��Է��ӣ�����ˮ�ķе����H2S����4��д��D��������SiO2������ᷴӦ����SiF4��ˮ����Ӧ�Ļ�ѧ����ʽΪ��SiO2+4HF=SiF4��+2H2O����5����ClO2������Mn2+�����ɺ�ɫ����MnO2��������13.50g ����0.2mol��ClO2ʱ����ת����1mol���ӣ����ݵ��ӵ�ʧ�غ��д����Ӧ�����ӷ���ʽΪ5Mn2++2ClO2+6H2O=2Cl��+5MnO2��+12H+��


 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д� ��ǰ�κ�ͬ����ϰϵ�д�
��ǰ�κ�ͬ����ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������У�����״���������������( )
A.P4
B.[SiO4]4��
C.CH4
D.CH3Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Ժ���չ�����ܵ���͵��ȡ������ʼ��仯����Ļ�ѧ�����������ơ�
��1����������ϡ��������,���ų�������д���������ᷴӦ�Ļ�ѧ����ʽ:_____________��
��2���ڸ��������������£�����NiC2O4ʹ��ֽ⣬���ܵõ�����ɫ������������д���÷�Ӧ�Ļ�ѧ����ʽ: _____________��
��3��Ni2O3������ˮ,���������Ტ�ų�������д���÷�Ӧ�����ӷ���ʽ: _____________��
��4�����������һ�ּ��Կɳ��������ȾС���������ϴ�������ص��ܷ�Ӧʽ��:H2+2NiO(OH) ![]() 2Ni(OH)2��д���ŵ�ʱ��������Ӧʽ: _____________��
2Ni(OH)2��д���ŵ�ʱ��������Ӧʽ: _____________��
��5�����ײ�������(Ni)��һ�ָ����ܵ缫���������Ʊ���������:
����I:ȡ0.2mol/L������������Һ������pH���������������̿���ˡ�
������:��������Һ�еμ�1.5mol/L��NaHCO3��ҺʹNi2+��ȫ����������:xNiCO3��yNi(OH)2��zH2O��
������:�������ij����ô����ߴ�ˮ��ϴ�������Ļ�˦�ɡ�
������:�����Թ���������Һ(N2H4��H2O)��ʹ����������ԭ��ȫ�������ɵ�Niˮϴ��������95%���Ҵ����ݺ����ɡ�Ϊ�ⶨxNiCO3��yNi(OH)2��zH2O���������������ʵ��:
��ȷ��ȡ7.54g��Ʒ�����������Һ(N2H4��H2O)��ַ�Ӧ�����ռ���1.12LN2��CO2�Ļ������(�ѻ���ɱ�״��)��
����ȡ����������Ʒ������գ���ȴ��Ƶò�������NiO������Ϊ4.5g��
ͨ������ȷ��xNiCO3��yNi(OH)2��zH2O�Ļ�ѧʽ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽд��ȷ����
A. ʯ��ʯ�ϵμ�ϡ����: CaCO3+2H+=Ca2++ H2O+CO2��
B. ���ˮ�еμ�FeCl3��Һ��Fe(OH)3����: Fe3++3H2O ![]() Fe(OH)3��+ 3H+
Fe(OH)3��+ 3H+
C. ����SO2ͨ��Ca(ClO)2��Һ��: SO2+ H2O + Ca2++ 2ClO-= CaSO3��+2HClO
D. ����ʯ��ˮ������С�մ���Һ���: Ca2++ OH-+ HCO3-=CaCO3��+ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������մ�Ҳ��һ�������մɲ��ϣ������������Ƴ������������������������ϵ�( )��
A.��������
B.��ѧ����
C.��ѧ����
D.���﹦��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���йز�����;��˵���в���ȷ����( )��
A.�������մɿ�������ѹ�ƵƵĵƹ�
B.�������մɿ������մɷ������IJ���
C.���ά������ң��ң�ء�������
D.�������մɿ������뵼�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2S ��һ�ִ�����Ⱦ���ҵ�ϲ�ȡ���ַ������������ŷš�
(1)��ҵ�Ͽɲ�ȡ������H2S ��������H2S ���ŷš�������H2S ��ԭ��Ϊ:H2S + Fe2(SO4)3= S��+ 2FeSO4 + H2SO4 4FeSO4 +O2 +2H2SO4 ![]() 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
�Իش���������:
����˾�����ʱ��FeSO4����������������ʱ5.0��105�����þ���������_________��
������ͼ1��ͼ2 �ж�ʹ����˾����������Ϊ_________������Ӧ�¶ȹ��ߣ���Ӧ�����½�����ԭ����____________��

(2) �ʻ���(COS) ����ʯ����ҵ�����������DZ���У���������������Ʊ�����֮һ��H2S ��COS �ڸ����·�����Ӧ: H2S(g)+CO2(g)![]() COS(g)+H2O(g) ��610K ʱ����0.40mol H2S ��0.10molCO2����2.5 L �Ŀո�ƿ�У�H2S��ƽ��ת�������¶ȵĹ�ϵ��ͼ��ʾ:
COS(g)+H2O(g) ��610K ʱ����0.40mol H2S ��0.10molCO2����2.5 L �Ŀո�ƿ�У�H2S��ƽ��ת�������¶ȵĹ�ϵ��ͼ��ʾ:
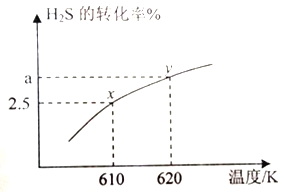
������˵���ܱ�����Ӧ�Ѵ�ƽ��״̬����__________��
A.H2S ��CO2�����ʵ���֮�ȱ��ֲ��� B.���������ܶȱ��ֲ���
C.��������ƽ����Է����������ٱ仯D.v��(H2S)=V��(COS)
���÷�Ӧ����H______0.(����>����<������=��)��x���Ӧ�¶��·�Ӧ��ƽ�ⳣ��K=_____(������λ��Ч����)��
����620K�ظ����飬��ƽ���ˮ�����ʵ�������Ϊ0.030.��H2S ��ת����a=_____%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ظı䣬�ᵼ��һ�����淴Ӧ��ƽ�ⳣ����ı�( )
A.ѹǿB.�¶�C.����D.��Ӧ��Ũ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com