
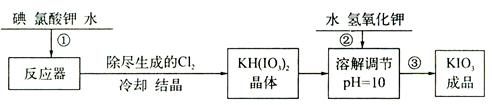
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3/100g水 | 8.08 | 12.6 | 18.3 | 24.8 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:实验题

| A.-2 | B.0 | C.+4 | D.+6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.约为5mL | B.大于25 mL | C.等于25 mL | D.小于25 mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②④⑤⑥ | B.②④⑤ | C.①③⑥ | D.④⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用酸性高锰酸钾溶液鉴别正己烷和乙醇 |
| B.用分液漏斗分离乙醛和水 |
| C.用苯、溴水和铁粉混合制取溴苯 |
| D.用米汤检验加碘盐中是否含碘元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
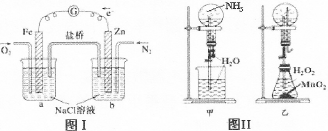
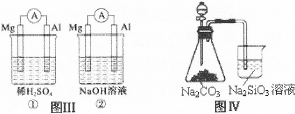
| A.图I装置中通入N2和O2的作用是相同的 |
| B.图Ⅱ中甲、乙两装置产生喷泉的原理一样 |
| C.图Ⅲ①装置中镁片是原电池的负极;②装置中镁片是原电池的正极 |
| D.图Ⅳ分液漏斗盛硝酸能证明非金属性N>C>Si,盛硫酸能证明非金属性S>C>Si |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.②④ | C.①③ | D.①②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
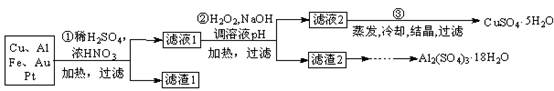

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用待测液润洗滴定用的锥形瓶 |
| B.配制FeCl3溶液时,向溶液中加入少量Fe和稀盐酸 |
| C.用稀硝酸酸洗涤盛做过银镜反应的试管 |
| D.液溴保存时液面覆盖一层水,装在带橡胶塞的试剂瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com