
| A | B | C | D |
 玻璃 |  氮化硅陶瓷 |  不锈钢 |  氧化铝制品 |
| 无机非金属材料 | 有机高分子材料 | 金属材料 | 耐火材料 |
| A、A | B、B | C、C | D、D |
科目:高中化学 来源: 题型:
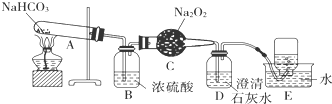
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.1 mol |
| B、0.87 mol |
| C、0.8 mol |
| D、0.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.l mol/L醋酸钙溶液中,c(Ca2+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、体积和pH都相同的NH4Cl溶液、盐酸,完全溶解少量且等质量的锌粉,前者所用时间少 |
| C、将n mol H2(g)、n mol I2(g)和2n mol H2 (g)、2n mol I2(g)分别充入两个恒温恒容的容器中,平衡时H2的转化率前者小于后者 |
| D、某物质的溶液中由水电离出的c(H+)=1×10-a mol?L-1,若a>7时,则该溶液的pH一定为14-a |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从海水提取物质都必须通过化学反应才能实现 |
| B、“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
| C、“绿色化学”的核心是利用化学原理进行环境治理 |
| D、生石灰、铁粉、硅胶是食品包装中常用的干燥剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A、0.1 mol?L-lNaHCO3溶液中各离子浓度的大小顺序为:c( Na+)>c(HCO3-)c(HJ-)>c(OH-) |
| B、少量的CO2通人到NaCN溶液中:CN-+H2O+CO2═HCN+HCO3- |
| C、用0.1 mol?L-l NaOH溶液中和等浓度的HCN溶液和HCOOH溶液时,前者所需NaOH溶液体积大 |
| D、相同体积的0.1 mol?L-l HCOONa溶液比0.1 mol?L-l NaCN溶液所含离子总数小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
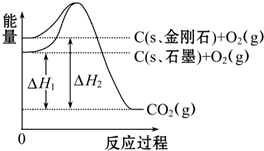
| A、C(s、石墨)═C(s、金刚石)△H=+1.9 kJ?mol-1 |
| B、石墨和金刚石的转化是物理变化 |
| C、金刚石的稳定性强于石墨 |
| D、1 mol石墨的能量比1 mol金刚石的总能量大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | 具有多种同素异形体,形成的化合物种类繁多 |
| Y | 短周期主族元素中原子半径最大 |
| Z | 位于元素周期表金属与非金属元素的分界线上,最高化合价为+4 |
| W | 富集在海水中的元素,它的某些化合物常用作消毒刹 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com