
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(SOCl2)中而形成的,电池总反应方程式为:8Li+3SOCl2===6LiCl+Li2SO3+2S,下列叙述中正确的是( )
A.电解质溶液中混入水,对电池反应无影响
B.金属锂作电池的正极,石墨作电池的负极
C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
D.电池工作过程中,金属锂提供的电子与正极区析出的硫的物质的量之比为4∶1
科目:高中化学 来源:2015-2016学年云南省高一下期末化学试卷(解析版) 题型:选择题
W、X、Y、Z均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为18。下列说法正确的是( )
A. 原子半径由大到小:Z>Y>X>W
B. 阴离子的还原性:Y>Z
C. 氢化物的沸点:Y>X
D. 氧化物对应水化物的酸性:Y<Z
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高二下期末化学试卷(解析版) 题型:选择题
下列有机化合物中均含有酸性杂质,除去这些杂质的方法中正确的是 ( )
A.苯中含苯酚杂质:加入溴水,过滤
B.乙醇中含乙酸杂质:加入碳酸钠溶液洗涤,分液
C.乙醛中含乙酸杂质:加入氢氧化钠溶液洗涤,分液
D.乙酸丁酯中含乙酸杂质:加入碳酸钠溶液洗涤,分液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一下期末化学试卷(解析版) 题型:选择题
某小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中p表示压强,T表示温度,n表示物质的量):

根据以上规律判断,下列结论正确的是( )
A.反应Ⅰ:ΔH>0,p2>p1
B.反应Ⅱ:ΔH>0,T1>T2
C.反应Ⅲ:ΔH>0,T2>T1;或ΔH<0,T2<T1
D.反应Ⅳ:ΔH<0,T2>T1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一下期末化学试卷(解析版) 题型:选择题
向一固定体积的密闭容器中通入a mol N2O4气体,在密闭容器内发生反应:N2O4(g)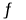 2NO2(g),达到平衡时再通入a mol N2O4气体,再次达到平衡时,与第一次达平衡时相比,N2O4的转化率( )
2NO2(g),达到平衡时再通入a mol N2O4气体,再次达到平衡时,与第一次达平衡时相比,N2O4的转化率( )
A.不变 B.增大 C.减小 D.无法判断
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一下期末化学试卷(解析版) 题型:选择题
下列有关的叙述正确的是( )
A. HClO是弱酸,所以NaClO是弱电解质
B. 向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
C. 根据分散质粒子的直径大小,分散系可分为溶液、浊液和胶体,浊液的分散质粒子大小介于溶液与胶体之间
D. “血液透析”原理与胶体的性质无关
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上期末化学试卷(解析版) 题型:填空题
(1)已知H-H 键能为436 kJ·mol-1,H-N键键能为391 kJ·mol-1,根据化学方程式: N2(g)+3 H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1。则N≡N键的键能是_________________
2NH3(g) ΔH=-92.4kJ·mol-1。则N≡N键的键能是_________________
(2)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是__________________。
A.C(s) + H2O(g) = CO(g) + H2(g) △H > 0
B.2H2(g)+O2(g)=2H2O(1) △H < 0
C.NaOH(aq) + HC1(aq) = NaC1(aq) + H2O(1) △H < 0
(3)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其正极的电极反应式___________。
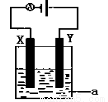
(4)电解原理在化学工业中有着广泛的应用。现将你设计的原电池通过导线与图中电解池相连,其中为 a电解液,X和Y均为惰性电极,则
①若a为CuSO4溶液,则电解时的化学反应方程式为 。
②若电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,当阳极产生的气体672mL(标准状况下)时,溶液的pH=_______(假设电解后溶液体积不变)。
③若用此电解装置模拟工业精炼铜,则应将a改为 溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上期末化学试卷(解析版) 题型:选择题
CO和H2在ThNi5作用下可以合成CH4。
已知温度为T时:① CO(g)+H2O(g) === CO2(g)+H2(g) ΔH=-41 kJ·mol-1
② CH4(g)+2H2O(g) === 4H2(g) + CO2(g) ΔH=+165 kJ·mol-1
下列说法不正确的是( )
A.催化剂不能改变该反应的ΔH
B.①中反应物的键能总和小于生成物的键能总和
C.②中反应物的总能量高于生成物的总能量
D.CO(g)与H2(g)合成CH4(g)的反应为放热反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期末化学试卷(解析版) 题型:选择题
共价键、离子键和范德瓦尔斯力都是微粒之间的不同作用力,下列含有上述两种结合力的是( )
①Na2O2 ②SiO2 ③石墨 ④金刚石 ⑤NaCl ⑥白磷.
A.①②④ B.①③⑥ C.②④⑥ D.③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com