
【题目】六种短周期元素在周期表中的相对位置如下所示,其中E元素原子核外电子总数是其最外层电子数的3倍。关于元素周期表及这六种元素性质,请回答:

(1)这六种元素的氢化物中,最稳定的是___________.(写化学式);
(2)AF2的结构式为_____________.
(3)在一定条件下,由B单质与H2反应生成1 molG气体时,放出的热量为46.2 kJ,写出该反应的热化学方程式:_____________________.
(4)工业上用G检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质B生成,写出化学方程式__________________________.该反应中被氧化的G与参与反应的G的质量之比__________.
(5)F的单质可由其氧化物与氢化物反应生成,写出该反应的化学方程式:__________.
【答案】 H2O S=C=S N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ/mol 8NH3+3Cl2=6NH4Cl+N2 1:4 2H2S+SO2=3S+2H2O
2NH3(g) ΔH=-92.4 kJ/mol 8NH3+3Cl2=6NH4Cl+N2 1:4 2H2S+SO2=3S+2H2O
【解析】由短周期元素相对位置,可知A、B、C处于第二周期,D、E、F处于第三周期,E元素原子核外电子总数是其最外层电子数的3倍,设核外最外层电子数为x,则有(2+8+x)=3x,解得x=5,则E为P元素,可知A为碳元素,B为N元素,C为O元素,D为Si,F为S元素。
(1)这六种元素中O元素非金属性最强,故氢化物中,最稳定的是H2O,故答案为:H2O;
(2)CS2与CO2结构相似,结构式为S=C=S,故答案为:S=C=S;
(3)在一定条件下,由氮气与H2反应生成1molG(氨气)时,放出的热量为46.2kJ,该反应的热化学方程式:N2(g)+3H2(g)2NH3(g)△H=-92.4 kJ/mol,故答案为:N2(g)+3H2(g)2NH3(g) △H=-92.4 kJ/mol;
(4)工业上用G(氨气)检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质B生成,反应生成氯化铵与氮气,反应方程式为:8NH3+3Cl2═6NH4Cl+N2,反应中被氧化的氨气与参与反应的氨气的质量之比为2:8=1:4,故答案为:8NH3+3Cl2═6NH4Cl+N2;1:4;
(5)F(硫)的单质可由其氧化物与氢化物反应生成,该反应的化学方程式:2H2S+SO2=3S↓+2H2O,故答案为:2H2S+SO2=3S↓+2H2O。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】化学式为C3H6Cl2的有机物,若再有一个氢原子被氯原子取代,则产物有两种可能的结构,原有机物的结构简式为( )
A.CH2Cl﹣CH2﹣CH2Cl
B.CHCl2﹣CH2﹣CH3
C.CH2Cl﹣CHCl﹣CH3
D.CH3﹣CCl2﹣CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法错误的是
A.碳酸氢钠可用于焙制糕点
B.木材纤维和土豆淀粉遇碘水均显蓝色
C.漂白粉可用于游泳池用水的消毒
D.聚乙烯塑料可用于制造包装材料、农用薄膜等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在恒容密闭容器中,进行反应:A(s)+2B(g)![]() 2C(g) ΔH<0。下列说法正确的是
2C(g) ΔH<0。下列说法正确的是
A. 达到平衡后,从容器中移走部分反应物A,则正反应速率将下降
B. 当混合气体的密度不再发生变化时,说明反应达到平衡状态
C. 改变反应前A与B的投料比,ΔH将发生相应的改变
D. 向反应体系中继续通入足量B气体,A有可能反应完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,将气体X、Y放入密闭容器中发生反应生成Z,5min后达到平衡.其初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/molL﹣1 | 0.1 | 0.2 | 0 |
平衡浓度/molL﹣1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是( )
A.该反应可表示为X+3Y2Z
B.反应达到平衡时,X的转化率为50%
C.前5min 以Y表示的平均反应速率为υ(Y)=0.01 molL﹣1min﹣1
D.增大压强使平衡向生成Z的方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. ![]() 由3种单体加聚得到
由3种单体加聚得到
B. 氨基酸溶于过量氢氧化钠溶液中生成的离子,在电场作用下向阴极移动
C. 甲苯与足量H2加成产物的一氯取代物有5种
D. 分子式为C4H6O2并能与饱和NaHCO3溶液反应生成CO2的有机物有3种(不含立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于放热反应H2 + Cl2 ![]() 2HCl下列说法中正确的是
2HCl下列说法中正确的是
A. 该反应中,化学能只转变为热能
B. 反应物所具有的总能量高于产物所具有的总能量
C. 产物所具有的总能量高于反应物所具有的总能量
D. 断开1mol H-H键和1mol Cl-Cl键所吸收的总能量小于形成2mol H-Cl键所放出的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,A、B、C、D、E、X是周期表给出元素组成的常见单质或化合物. 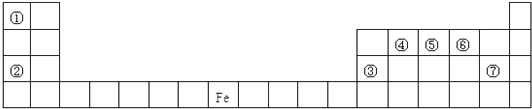
已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去)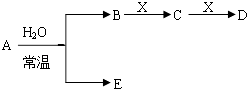
(1)若E为氧化物,则A与水反应的化学方程式为 , ①当X是碱性盐溶液,C分子中有22个电子时,表示X呈碱性的离子方程式为 ②当X为金属单质时,则X与B的稀溶液反应生成C的离子反应方程式为
(2)若E为单质气体,D为白色沉淀,A的化学式可能是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表为元素周期表的一部分,针对表中的①~⑨九种元素,请回答有关问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
4 | ⑧ | ⑨ |
(1)⑨的元素符号是 .
(2)在这些元素中,化学性质最不活泼的原子结构示意图为 .
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是(填化学式,下同),碱性最强的是 , 显两性的是 .
(4)将元素①与氢元素组成的最简单有机物和⑥的单质按1:1混合后的气体在光照条件下放置一段时间,最多能得到产物.
(5)用电子式表示④和⑥两元素形成化合物的过程为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com