
【题目】已知293K时下列物质的溶度积![]() 单位已省略
单位已省略![]() :
:
| Ag2SO4 | FeS | CuS | Ag2S |
| 1.2×10-5 | 6.3×10-18 | 8.5×10-45 | 6.3×10-50 |
下列说法正确的是![]()
![]()
A.相同温度下,Ag2SO4、FeS、CuS饱和溶液中:![]()
B.向FeS悬浊液中滴加CuSO4溶液发生反应的离子方程式:![]()
C.浓度均为0.004mol/L的AgNO3和H2SO4溶液等体积混合后不能产生沉淀
D.向饱和Ag2S溶液中加少量Na2S固体,溶液中c(Ag+)不变
【答案】C
【解析】
A.根据溶度积计算c(Ag+)、c(Fe2+)和c(Cu2+),进一步比较浓度的大小关系;
B. FeS为沉淀,书写离子方程式时要保留化学式;
C. Qc(Ag2SO4)=c2(Ag+)c(SO42-),根据Qc与Ksp的大小判断;
D. 根据Ksp= c2(Ag+)c(S2-)判断。
A. c(Ag+)=![]() =3×10-
=3×10-![]() mol/L,c(Fe2+)=
mol/L,c(Fe2+)=![]() =2.51×10-9 mol/L,c(Cu2+)=
=2.51×10-9 mol/L,c(Cu2+)=![]() =9.22×10-24 mol/L,因此c(Ag+)>c(Fe2+)>c(Cu2+),A项错误;
=9.22×10-24 mol/L,因此c(Ag+)>c(Fe2+)>c(Cu2+),A项错误;
B. FeS悬浊液中滴加CuSO4溶液发生反应的离子方程式为:![]() ,B项错误;
,B项错误;
C. 浓度均为0.004mol/L的AgNO3和H2SO4溶液等体积混合,混合后c(Ag+)=c(SO42-)=0.002mol/L,Qc(Ag2SO4)=c2(Ag+)c(SO42-)=(0.002)2×0.002=8×10-9,而293K时Ksp(Ag2SO4)= 1.2×10-5,Qc(Ag2SO4)< Ksp(Ag2SO4),反应向沉淀溶解的方向移动,不能产生沉淀,C项正确;
D. 温度不变Ksp不变,由Ksp(Ag2S)=c2(Ag+)c(S2-)可知,向饱和Ag2S溶液中加少量Na2S固体,c(S2-)增大,c(Ag+)减小,D项错误;
答案选C。


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】G是药物中间体,其部分合成路线如下:

已知:RCHO+CH3COR1![]() RCH=CHOR1+H2O
RCH=CHOR1+H2O
请回答下列问题:
⑴D所含官能团有醚键、羟基和________。试剂E的名称是________。
⑵C→D的反应类型为________。G的分子式为________。
⑶写出A→B的化学方程式________。
⑷在上述方案中,设计A→B、C→D步骤的目的是________。
⑸芳香族化合物T是D的同分异构体,T同时具备下列条件的结构有________种。
①能发生银镜反应;
②遇FeCl3溶液不发生显色反应,但其在稀硫酸中水解的产物之一遇FeCl3溶液能发生显色反应。其中,在核磁共振氢谱上有4组峰的T的结构简式为________。
⑹以环己醇和 为原料,设计合成
为原料,设计合成 路线
路线![]() 无机试剂自选
无机试剂自选![]() :________。
:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭容器中,能表示反应X(g)+2Y(g) ![]() 2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比是1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
A. ①②B. ①④C. ②③D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应![]() 在5L的密闭容器中进行,0~30s内,C的物质的量增加了0.30mol。下列叙述正确的是( )
在5L的密闭容器中进行,0~30s内,C的物质的量增加了0.30mol。下列叙述正确的是( )
A.容器中D的物质的量至少为0.45mol
B.0~30s内,A的平均反应速率是0.010 mol·L-1·s-1
C.容器中A、B、C、D的物质的量之比一定是4:5:4:6
D.容器中A的物质的量一定增加了0.30mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种直接铁燃料电池(电池反应为:3Fe + 2O2=Fe3O4)的装置如图所示,下列说法正确的是

A. Fe极为电池正极
B. KOH溶液为电池的电解质溶液
C. 电子由多孔碳极沿导线流向Fe极
D. 每5.6gFe参与反应,导线中流过1.204×1023个e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丙叉环丙烷(b)由于其特殊的结构,一直受到化学家的重视,根据其转化关系(如图),下列说法正确的是
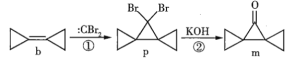
A.b的所有原子都在同一个平面内
B.b可以发生加成、氧化、加聚反应
C.p在氢氧化钠的醇溶液中加热生成烯烃
D.m的同分异构体中属于芳香化合物的共有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,正确的是( )
A.甲烷燃烧热为890.3 kJmol-1,热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=+890.3 kJmolˉ1
B.稀盐酸和稀氢氧化钠溶液混合,其热化学方程式为:H++OH-=H2O △H=-57.3 kJmolˉ1
C.H2燃烧热为285.8kJmolˉ1,燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(1) △H=-571.6 kJmolˉ1
D.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6 kJ·mol-1
2NH3(g) △H=-38.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正丁醇常用作有机反应的溶剂。实验室制备正丁醚的主要实验装置如图:
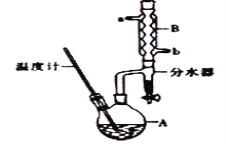
反应物和产物的相关数据如表:
相对分子质量 | 沸点/℃ | 密度(g.cm-3) | 水中溶解性 | |
正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |
合成正丁醚的步骤:
①将6mL浓硫酸和37g正丁醇,按一定顺序添加到A中,并加几粒沸石。
②加热A中反应液,迅速升温至135℃,维持反应一段时间,分离提纯;
③待A中液体冷却后将其缓慢倒入盛有70mL水的分液漏斗中,振摇后静置,分液得粗产物。
④粗产物依次用40mL水、20mLNaOH溶液和40mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙。
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚13g。
请回答:
(1)加热A前,需先从_________(填“a”或“b”)口向B中通入水。
(2)写出步骤②中制备正丁醚的化学方程式____________________________________。
(3)步骤③的目的是初步洗去____________________,振摇后静置,粗产物应从分液漏斗的_____(填“上”或“下”)口分离出。
(4)步骤④中最后一次水洗的目的为_______________________________________。
(5)步骤⑤中,加热蒸馏时应收集________(填选项字母)左右的馏分。
a.100℃b.117℃c.135℃d.142℃
(6)本实验中,正丁醚的产率为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述正确的是
![]() 浓硝酸通常保存在棕色试剂瓶中
浓硝酸通常保存在棕色试剂瓶中
![]() 检验亚硫酸钠溶液在空气中放置是否变质可以先加硝酸溶液,再加氯化钡溶液来检验
检验亚硫酸钠溶液在空气中放置是否变质可以先加硝酸溶液,再加氯化钡溶液来检验
![]() 锌与稀硝酸反应可以得到氢气
锌与稀硝酸反应可以得到氢气
![]() 足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
![]() 浓硫酸滴到纸张上变黑,说明浓硫酸具有脱水性
浓硫酸滴到纸张上变黑,说明浓硫酸具有脱水性
![]() 浓硫酸使胆矾变白,说明浓硫酸具有脱水性
浓硫酸使胆矾变白,说明浓硫酸具有脱水性
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com