
下列关于有机物因果关系的叙述中,完全正确的一组是( )
选项原因结论
A乙烯和苯都能使溴水褪色苯和乙烯都能与溴水发生加成反应
B乙酸分子中含有羧基可与NaHCO3溶液反应生成CO2
C纤维素和淀粉的化学式均为(C6H10O5)n它们属于同分异构体
D乙酸乙酯和乙烯在一定条件下都能与水反应两者属于同一反应类型
科目:高中化学 来源:2014高考化学苏教版总复习 专题10化学实验基础练习卷(解析版) 题型:实验题
已知某酸性土壤浸取液中除Fe3+外,还含有一定量Mg2+和Al3+。请设计合理实验检验该浸取液中的Mg2+、Al3+。
限选实验用品与试剂;烧杯、试管、玻璃棒、滴管、玻璃片、pH试纸;浸取液、20%KSCN、0.1 mol·L-1 NaOH、6 mol·L-1 NaOH、0.1 mol·L-1 HCl、蒸馏水。
必要时可参考:
沉淀物 | 开始沉淀时的pH | 沉淀完全时的pH |
Mg(OH)2 | 9.6 | 11.1 |
Fe(OH)3 | 2.7 | 3.7 |
根据你设计的实验方案,叙述实验操作、预期现象和结论。(测定溶液pH的具体操作可不写)
实验操作 | 预期现象和结论 |
步骤1: |
|
步骤2: |
|
步骤3: |
|
…… |
|
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 离子反应练习卷(解析版) 题型:选择题
下列离子方程式表达正确的是( )
A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+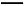 Fe3++3H2O
Fe3++3H2O
B.小苏打溶液呈碱性的原因:HC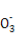 +H2O
+H2O H3O++C
H3O++C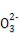
C.稀硝酸中加入足量的铁屑:3Fe+8H++2N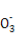
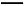 3Fe2++2NO↑+4H2O
3Fe2++2NO↑+4H2O
D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液:N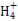 +Al3++2S
+Al3++2S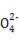 +2Ba2++5OH-
+2Ba2++5OH-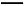 Al
Al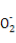 +2BaSO4↓+NH3·H2O+2H2O
+2BaSO4↓+NH3·H2O+2H2O
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 电解质溶液练习卷(解析版) 题型:选择题
今有室温下四种溶液,有关叙述不正确的是( )
| ① | ② | ③ | ④ |
pH | 11 | 11 | 3 | 3 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A.①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
B.分别加水稀释10倍,四种溶液的pH:①>②>④>③
C.①、④两溶液等体积混合,所得溶液中c(Cl-)>c(N )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
D.Va L ④与Vb L ②溶液混合,若混合后溶液pH=4,则Va∶Vb=11∶9
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 电解质溶液练习卷(解析版) 题型:选择题
已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+。欲使平衡发生如图变化,可以采取的措施是( )
CH3COO-+H+。欲使平衡发生如图变化,可以采取的措施是( )
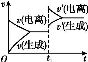
A.加少量烧碱溶液 B.升高温度
C.加少量冰醋酸 D.加水
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 有机物组成练习卷(解析版) 题型:选择题
下列各组中的反应,属于同一反应类型的是( )
A.乙烷和氯气制氯乙烷;乙烯与氯化氢反应制氯乙烷
B.乙醇和乙酸制乙酸乙酯;苯的硝化反应
C.葡萄糖与新制氢氧化铜共热;蔗糖与稀硫酸共热
D.乙醇和氧气制乙醛;苯和氢气制环己烷
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 实验基础练习卷(解析版) 题型:选择题
下列说法正确的是( )
A.实验室里需要480 mL 2.0 mol/L的氢氧化钠溶液,配制溶液时先称量氢氧化钠固体38.4 g,然后再按照溶解、冷却、洗涤、定容、摇匀的步骤进行操作
B.用标准盐酸滴定NaOH溶液测其浓度时,酸式滴定管用蒸馏水洗涤后,没用标准盐酸润洗,直接装标准盐酸滴定,所测的碱液浓度偏低
C.蒸发硫酸铜溶液时蒸发皿放在石棉网上加热,并用坩埚钳夹取蒸发皿
D.向氢氧化铁胶体中逐滴加入稀硫酸,先出现红褐色沉淀,继续滴加稀硫酸,沉淀溶解得到黄色溶液
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 化学反应中的能量变化练习卷(解析版) 题型:选择题
将如图所示实验装置的K闭合,下列判断正确的是( )
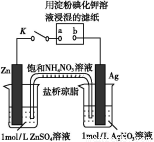
A.Ag电极上发生氧化反应
B.盐桥中N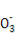 向Zn电极移动
向Zn电极移动
C.电子沿Zn→a→b→Ag路径流动
D.片刻后可观察到滤纸a点变蓝
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 物质结构与性质练习卷(解析版) 题型:填空题
第4周期元素由于受3d能级电子的影响,性质的递变规律与短周期元素略有不同。
Ⅰ.第4周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。镓(31Ga)的基态原子的电子排布式是 ;31Ga的第一电离能却明显低于30Zn的,原因是
。
Ⅱ.第4周期过渡元素的明显特征是形成多种多样的配合物。
(1)CO和NH3可以和很多过渡金属形成配合物。CO与N2互为等电子体,CO分子中C原子上有一对孤电子对,C、O原子都符合8电子稳定结构,则CO的结构式可表示为 。NH3分子中N原子的杂化方式为 杂化,NH3分子的空间立体构型是 。
(2)如图甲所示为二维平面晶体示意图,所表示的化学式为AX3的是 。
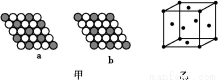
(3)图乙为一个铜晶胞,此晶胞立方体的边长为a cm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则阿伏加德罗常数可表示为 mol-1(用含a、ρ的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com