
A.NaNO3、NaHSO4、CH3COONa? B.MgSO4、AlCl3、NaAlO2?
C.Ba(NO3)2、FeSO4、NH4HSO4? D.Na2SO3、Na2SO4、BaCl2?
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
| 反应阶段 | Ⅰ | Ⅱ | Ⅲ |
| 盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现 象 | 无气体 | 有气体 | 无气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
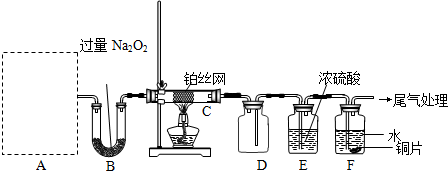


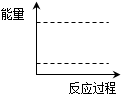
查看答案和解析>>
科目:高中化学 来源: 题型:
将下列固体混合物溶于足量蒸馏水中,既能发生复分解反应,又能发生氧化还原反应的是( )?
A.NaNO3、NaHSO4、CH3COONa?
B.MgSO4、AlCl3、NaAlO2?
C.Ba(NO3)2、FeSO4、NH4HSO4?
D.Na2SO3、Na2SO4、BaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com