
| 实验编号 | T/℃ | 大理石规格 | HNO3浓度/mol•L-1 |
| ① | 常温 | 细颗粒 | 2.00 |
| ② | 常温 | 细颗粒 | 1.00 |
| ③ | 35℃ | 粗颗粒 | 2.00 |
| ④ | 35℃ | 细颗粒 | 2.00 |
分析 (1)由信息可知,硝酸的浓度不同、大理石的接触面积不同、温度不同;
(2)①②只控制浓度不同,③④控制接触面积不同;
(3)由控制变量法可知,硝酸溶液的体积、固体的质量不变;
(4)①测定反应速率需要测定时间;
②干燥管吸收水,排出二氧化碳气体,前后的质量差为气体的质量;
③若撤除干燥管装置,气体的质量偏大.
解答 解:(1)由信息可知,硝酸的浓度不同、大理石的接触面积不同、温度不同,则可完成硝酸浓度、温度、大理石表面积对速率影响,
故答案为:硝酸浓度、温度、大理石表面积;
(2)①②只控制浓度不同,③④控制接触面积不同,则②为常温,③为粗颗粒,④为细颗粒,故答案为:
| 实验编号 | T/℃ | 大理石规格 | HNO3浓度/mol•L-1 |
| ① | |||
| ② | 常温 | ||
| ③ | 粗颗粒 | ||
| ④ | 细颗粒 |
点评 本题考查反应速率的实验探究,为高频考点,把握温度、浓度、接触面积对反应速率的影响为解答的关键,侧重分析与实验能力的考查,注意控制变量法的应用,题目难度不大.


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L的NH4Cl溶液:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | 0.1mol/L的CH3COONa:c(CH3COOH)>c(H+)>c(CH3COO-)>c(OH-) | |
| C. | 某FeCl3溶液pH=4:c(Cl-)>c(H+)>c(Fe3+)>c(OH-) | |
| D. | 某弱酸的酸式盐NaHA溶液中一定有:c(OH-)+2c(A2-)═c(H+)+c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易 | |
| B. | 卤化氢的稳定性按HF、HCl、HBr、HI的顺序依次增大 | |
| C. | 卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱 | |
| D. | 卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
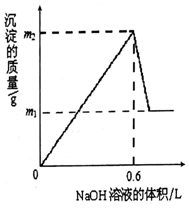 将m1g铜铝合金投入到1LH2SO4和HNO3的混合溶液中,完全溶解后只生成VLNO气体(标准状况),向反应后的溶液中逐渐加入1mol/LNaOH溶液,生成沉淀的质量与所加NaOH溶液的体积的关系如图所示.下列说法中不正确的是( )
将m1g铜铝合金投入到1LH2SO4和HNO3的混合溶液中,完全溶解后只生成VLNO气体(标准状况),向反应后的溶液中逐渐加入1mol/LNaOH溶液,生成沉淀的质量与所加NaOH溶液的体积的关系如图所示.下列说法中不正确的是( )| A. | m1-m2═10.2 | B. | 2c(H2SO4)+c(HNO3)═0.8 mol•L-1 | ||
| C. | 原合金中铝的质量分数为34.7% | D. | V=2.24 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
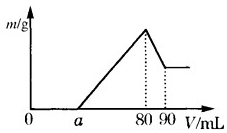 (1)把一定质量的镁、铝混合物投入到 2mol•L-1 的盐酸中,待金属完全溶解后,向溶液中加入 2mol•L-1 的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示.则:
(1)把一定质量的镁、铝混合物投入到 2mol•L-1 的盐酸中,待金属完全溶解后,向溶液中加入 2mol•L-1 的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示.则:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3FeO+10HNO3═3Fe(NO3)3+NO↑+5H2O | B. | C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O | ||
| C. | Al(OH)3+3HNO3═Al(NO3)3+3H2O | D. | 3Zn+8HNO3═3Zn(NO3)2+2NO↑+4H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com