
| A. | Na2O2、NaClO中所含化学键类型完全相同 | |
| B. | 只有活泼金属与活泼非金属元素之间才能形成离子键 | |
| C. | D2O和T2O是同一物质 | |
| D. | 氯气与NaOH反应的过程中,同时又离子键、极性键和非极性键的断裂和形成 |
分析 A.Na2O2含离子键和O-O非极性键,NaClO中含离子键和Cl-O极性键;
B.铵盐中含离子键,均为非金属元素;
C.D2O和T2O均为水;
D.氯气与NaOH反应生成NaClO、NaCl、H2O,产物中不存在非极性键.
解答 解:A.Na2O2含离子键和O-O非极性键,NaClO中含离子键和Cl-O极性键,则化学键不完全相同,故A错误;
B.铵盐中含离子键,均为非金属元素,离子键的形成中可能不含金属元素,故B错误;
C.D2O和T2O均为水,是同种物质,故C正确;
D.氯气与NaOH反应生成NaClO、NaCl、H2O,产物中不存在非极性键,则离子键、极性键和非极性键的断裂,但没有非极性键的形成,故D错误;
故选C.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答本题关键,侧重分析与应用能力的考查,注意常见物质中的化学键及结合实例分析解答,题目难度不大.


 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 与等体积、pH=3的盐酸比较,跟足量锌粒反应产生的H2更少 | |
| B. | 加水稀释到原体积的10倍后溶液pH变为4 | |
| C. | 加入少量乙酸钠固体,溶液pH升高 | |
| D. | 升高温度,溶液中所有离子浓度均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
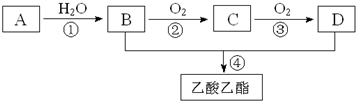
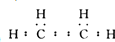 ,其空间构型平面形.
,其空间构型平面形.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
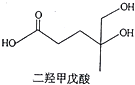 二羟甲戊酸是生物合成青蒿素的原料之一,下列关于二羟甲戊酸的说法正确的是( )
二羟甲戊酸是生物合成青蒿素的原料之一,下列关于二羟甲戊酸的说法正确的是( )| A. | 与乙醇发生酯化反应生成产物的分子式为C8H18O4 | |
| B. | 能发生加成反应,不能发生取代反应 | |
| C. | 在铜的催化下与氧气反应的产物可以发生银镜反应 | |
| D. | 标准状况下1mol该有机物可以与足量金属钠反应产生22.4L H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2的用途广泛,主要用途是用于做半导体材料 | |
| B. | SiO2不与任何酸或碱性性氧化物反应 | |
| C. | SiO2和CO2的结构不同,但它们都具有氧化性,都能与强碱反应 | |
| D. | 因为高温时二氧化硅与碳酸钠反应放出CO2,所以硅酸的酸性比碳酸强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸乙酯中含乙酸杂质:加入饱和碳酸钠溶液洗涤,分液 | |
| B. | 乙醇中含乙酸杂质:加入碳酸钠溶液洗涤,分液 | |
| C. | 乙醛中含乙酸杂质:加入氢氧化钠溶液洗涤,分液 | |
| D. | 苯中含苯酚杂质:加入浓溴水,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在纯水中加入少量硫酸或硫酸铵,均可抑制水的电离 | |
| B. | 电解质越弱,则其溶液的导电能力就越差 | |
| C. | 在白色ZnS沉淀上滴CuSO4溶液,沉淀变黑,说明相同条件下溶解度CuS比ZnS更小 | |
| D. | 加热NaR溶液时,溶液的pH变小,证明HR为弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | M | N | 除杂试剂 | 除杂方法 |
| A | C2H5OH | H2O | 生石灰 | 蒸馏 |
| B | CH4 | CH2═CH2 | 酸性KMnO4溶液 | 洗气 |
| C | CH3COOCH2CH3 | CH3COOH、C2H5OH | NaOH溶液 | 分液 |
| D | 苯酚 | 三溴苯酚 | 水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
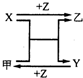 回答下列问题:
回答下列问题: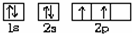 ,乙的电子式为
,乙的电子式为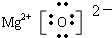 .
.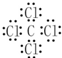 ,乙的化学式为NaCl.
,乙的化学式为NaCl.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com