
| A. | Na+、H+、Cl-、HCO3- | B. | Na+、Fe2+、Cl-、OH- | ||
| C. | NH4+、CO32-、NO3-、Ba2+ | D. | Cu2+、Fe3+、Mg2+、SO42- |
分析 A.碳酸氢根离子与氢离子反应;
B.亚铁离子与氢氧根离子反应生成氢氧化亚铁沉淀;
C.碳酸根离子与钡离子反应生成难溶物碳酸钡;
D.四种离子之间不发生反应,能够共存.
解答 解:A.H+、HCO3-之间发生反应,在溶液中不能大量共存,故A错误;
B.Fe2+、OH-之间反应生成氢氧化亚铁,在溶液中不能大量共存,故B错误;
C.CO32-、Ba2+之间反应生成碳酸钡沉淀,在溶液中不能大量共存,故C错误;
D.Cu2+、Fe3+、Mg2+、SO42-之间不反应,在溶液中可以大量共存,故D正确;
故选D.
点评 本题考查离子共存的正误判断,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;试题侧重对学生基础知识的训练和检验,有利于培养学生灵活运用基础知识解决实际问题的能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=0的溶液:Fe2+、Mg2+、NO3-、SO42- | |
| B. | 由水电离出的c(H+)=1×10-13mol/L的溶液:Al3+、K+、SO42-、Cl- | |
| C. | $\frac{c({OH}^{-})}{c({H}^{+})}$=1012的溶液中:NH4+、Al3+、NO3-、CO32- | |
| D. | pH=14的溶液:Na+、K+、Al3+、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铁的化学式为FeSO4 | |
| B. | 氧离子结构示意图: | |
| C. | 碳酸氢钠的电离方程式 NaHCO3═Na++HCO3- | |
| D. | 质量数为37的氯核素符号:${\;}_{37}^{17}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.25mol | B. | 0.30mol | C. | 0.35mol | D. | 0.4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
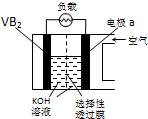 硼化钒(VB2)-空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时反应为:4VB2+11O2═4B2O3+2V2O5.下列说法正确的是( )
硼化钒(VB2)-空气电池是目前储电能力最高的电池,电池示意图如图所示,该电池工作时反应为:4VB2+11O2═4B2O3+2V2O5.下列说法正确的是( )| A. | 电极a为电池正极 | |
| B. | 图中选择性透过膜只能让阳离子选择性透过 | |
| C. | 电子由VB2极经KOH溶液流向a电极 | |
| D. | VB2极发生的电极反应为:2VB2+22OH--22e-═V2O5+2B2O3+11H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸溶液与NaOH溶液相混合后,所得溶液呈中性:c(Na+)>c(CH3COO-) | |
| B. | 浓度为0.1 mol•L-1的碳酸钠溶液:c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | pH=12的氨水溶液与pH=2的盐酸等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | 等物质的量的氨水和盐酸混合后的溶液:c(H+)=c(OH-)+c(NH3•H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
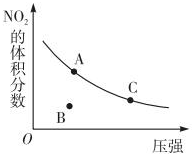
| A. | A、C两点的反应速率:v(A)>v(C) | |
| B. | A、C两点气体的颜色:A深,C浅 | |
| C. | B点正逆反应速率:v(正)>v(逆) | |
| D. | A、C两点气体的平均相对分子质量:A>C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g) 在反应中被氧化为1mol SO3(g) 的△H=-99kJ/mol.回答下列问题:
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g) 在反应中被氧化为1mol SO3(g) 的△H=-99kJ/mol.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com