
燃料电池的设计原理是基于将燃料燃烧时的化学能转变为电能,所以凡是燃料的燃烧反应从原理上说都可以设计成原电池反应,下列说法正确的是( )
|
| A. | 燃料电池工作时O2在正极上发生氧化反应 |
|
| B. | 燃料电池工作时O2在负极上发生氧化反应 |
|
| C. | 燃料电池工作时燃料在负极上发生还原反应 |
|
| D. | 燃料电池若以KOH溶液为介质,则工作时不会产生CO2气体 |
| 化学电源新型电池. | |
| 专题: | 电化学专题. |
| 分析: | A、燃料电池正极上发生还原反应; B、燃料电池O2在正极上发生还原反应; C、燃料电池工作时燃料在负极上发生氧化反应; D、碱和二氧化碳反应生成碳酸根离子. |
| 解答: | 解:A、燃料电池工作时O2在正极上发生还原反应,故A错误; B、燃料电池工作时O2在正极上发生还原反应,故B错误; C、燃料电池工作时燃料在负极上发生氧化反应,故C错误; D、燃料电池若以KOH溶液为介质,则工作时不会产生CO2气体,得到的是碳酸根离子,故D正确. 故选D. |
| 点评: | 本题考查学生原电池的工作原理知识,注意知识的归纳和梳理是解题的关键,难度中等. |


科目:高中化学 来源: 题型:
足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和NO2、NO的混合气体4.48 L
(标准状况),这些气体与一定体积O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是60 mL,下列说法不正确的是( )
A.参加反应的硝酸是0.5 mol
B.消耗氧气的体积为1.68 L
C.此反应过程中转移的电子为0.6 mol
D.混合气体中含NO2 3.36 L
查看答案和解析>>
科目:高中化学 来源: 题型:
只用一种试剂即可鉴别乙醇、乙醛、乙酸、甲酸等有机物的溶液,这种试剂是( )
|
| A. | 新制生石灰 | B. | 酸性高锰酸钾溶液 |
|
| C. | 浓溴水 | D. | 新制Cu(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列三种化合物的结构简式:

请认真观察后回答下列问题:
(1)写出肉桂酸分子中官能团的名称: .
(2)以上三种化合物中不能够和NaHCO3溶液反应生成CO2的是 (写名称).
(3)乙酰水杨酸与NaOH溶液反应,1mol该有机物最多可消耗NaOH mol,其反应方程式为: .
(4)可用于鉴别以上三种化合物的一组试剂是 .
①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液 ④氢氧化钠溶液
A.②与③B.②与④C.①与④D.①与②
查看答案和解析>>
科目:高中化学 来源: 题型:
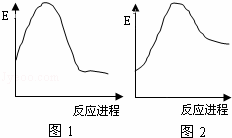
图中E表示反应物或生成物的能量,下列说法正确的是( )
|
| A. | 图1可表示C+O2→CO2的能量变化过程 |
|
| B. | 图1可表示CaCO3→CaO+CO2的能量变化过程 |
|
| C. | 图2可表示Mg+2HCl→MgCl2+H2 的能量变化过程 |
|
| D. | 图1表示的反应是吸热反应,图2表示的反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y两种金属,下列能说明X的金属性强于Y的金属性的组合是( )
①X的最高价氧化物的水化物的碱性强于Y的最高价氧化物的水化物的碱性
②X能置换出CuSO4溶液中的Cu,Y投入CuSO4溶液中无任何现象出现
③将X、Y用导线连接一起插入H2SO4溶液中,Y上冒大量气泡
④用碳棒电极电解含X、Y两种金属离子的盐溶液时,一开始析出的是金属Y
⑤X单质能从Y的硫酸盐溶液中置换出Y单质.
|
| A. | ①④⑤ | B. | ①②③⑤ | C. | ①③④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知R2﹣的核内有x个中子,R的质量数为M,则m g R2﹣含有电子的物质的量为( )
|
| A. | (M﹣x+2)mol | B. |
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为: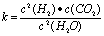 它所对应的化学反应为:
它所对应的化学反应为:
(2)—定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器中,发生(1)中反应:其相关数据如下表所示:
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | |
| C(s) | H2O(g) | H2(g) | ||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 8 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3 |
①T1℃时,该反应的平衡常数K=
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度 (填选项字母)。
A. =0.8 mol·L-1 B. =1.4 mol·L-1 C. <1.4 mol·L-1 D. >1.4 mol·L-1
③丙容器的容积为1L,T1℃时,按下列配比充入C(s)、H2O(g)、CO2(g)和H2(g), 达到平衡时各气体的体积分数与甲容器完全相同的是 (填选项字母)。
A. 0.6 mol 1.0 mol 0.5 mol 1.0 mol B. 0.6 mol 2.0 mol 0 mol 0 mol
C. 1.0 mol 2.0 mol 1.0 mol 2.0 mol D. 0.25 mol 0.5 mol 0.75 mol 1.5 mol
(3)将燃煤废气中的CO2转化为甲醚的反应原理为:
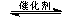 2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g)
2CO2(g) + 6H2(g) CH3OCH3(g) + 3H2O(g)
已知一定压强下,该反应在不同温度、不同投料比时,CO2的转化率见下表:
| 投料比[n(H2) / n(CO2)] | 500 K | 600 K | 700 K | 800 K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
①该反应的焓变△H 0,熵变△S 0(填>、<或=)。
②用甲醚作为燃料电池原料,在碱性介质中该电池负极的电极反应式 。
若以1.12 L·min-1(标准状况)的速率向该电池中通入甲醚(沸点为-24.9 ℃),用该电池电解500 mL 2 mol·L-1 CuSO4溶液,通电0.50 min后,理论上可析出金属铜
g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com