
【题目】水溶液中能大量共存的一组离子是( )
A.Na+、Al3+、Cl﹣、CO32﹣
B.H+、Na+、Fe2+、MnO4﹣
C.K+、Ca2+、Cl﹣、NO3﹣
D.K+、NH4+、OH﹣、SO42﹣
科目:高中化学 来源: 题型:
【题目】下列关于营养物质的说法,不正确的是
A. 油脂属于天然高分子 B. 纤维素能水解为葡萄糖
C. 鸡蛋煮熟过程中蛋白质变性 D. 食用新鲜蔬菜和水果可补充维生素C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置和有关数据如下:

相对分子质量 | 密度/(g·cm3) | 沸点/℃ | 水中溶解性 | |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 112 | 难溶 |
实验步骤:
在A 中加入4.40g异戊醇、6.00g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯4.55g。
请回答下列问题:
(1)仪器B的名称是_____;B中冷却水是从_____(填“下口”或“上口”)流进的。
(2)加入碎瓷片的作用是_______;如果加热一段时间后发现忘记加瓷片,应该采取的操作是_____________________。
(3)在洗涤、分液操作中,第二次洗涤,用饱和碳酸氢钠溶液洗涤的主要目的是_______,不能用NaOH溶液洗涤的原因是___________。第二次洗涤后,充分振荡,然后静置,待分层后,产物应该从分液漏斗的_______(填“上口倒出”或“下口放出”)。
(4)在蒸馏操作中,仪器选择及安装都正确的是下图中的_____(填字母标号),若从130℃ 便开始收集馏分,会使实验的产率______(填“偏高”、“偏低”或“无影响”)。

(5)水的沸点为100℃,比乙酸异戊酯低42℃ ,但仍要先加入MgSO4后过滤再蒸馏,而不是直接蒸馏。结合题中信息分析,下列说法正确的是______(填字母)。
A.水可能会与乙酸异戊酯形成一种“恒沸溶液”(在溶液的某一组成时,在某温度下,混合液同时汽化或同时冷凝),不能进一步提纯,所以要先用MgSO4干燥
B.在加入MgSO4后如不先过滤就蒸馏,加热时硫酸镁的结晶水合物又会脱水
C.如不先用MgSO4吸收水分,蒸馏时水先被蒸出,浪费能源和延长蒸馏时间
D.本实验中要乙酸过量,而不是异戊醇过量,可能的原因是异戊醇比乙酸价格贵;另外异戊醇过量时,异戊醇与乙酸异戊酯沸点相近(小于30℃),蒸馏时完全分离困难
(6)将乙酸异戊酯中的异戊醇除去,是在哪个步骤中除去的______(填字母)。
A.在第一次水洗和后面的分液中除去的
B.在第二次用饱和碳酸氢钠溶液洗涤和后面的分液中除去的
C.在“过滤”中除去的
D.由于本实验中加入过量乙酸,异戊醇已经反应完全,所以不需除杂(异戊醇)了
E.在最后的“蒸馏”步骤中除去的
(7)产物乙酸异戊酯的产率是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分离方法错误的是( )
A.用过滤的方法除去食盐水中的泥沙 B.用酒精萃取碘水中的碘
C.用蒸馏的方法将自来水制成蒸馏水 D.用分液的方法分离花生油与水的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是短周期中原子序数依次增大的4种元素,W与Y、X与Z处于同期表同一主族,W元素以W-W链化合物构成了生命界,Y元素以Y-X-Y链化合物构成了矿物界。
(1)W原子价电子的轨道表达式为_____________。
(2)WX的等电子体有N2、_______等。WN-与WX均为配合物中常见的配体,WN-作配体时,提供孤电子对的通常是W原子而不是氮原子,其原因是_________。
(3)ZX2的空间构型是______________。
(4)YF4遇水易发生水解,水解后产生的HF与部分YF4生成配离子YF62-,其反应的化学方程式为:3YF4+4H2O=H4YO4+2H2YF6。该反应混合物中,中心原子杂化方式相同的分子是_________。
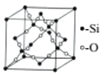
(5)一种石英晶体的晶胞结构如图所示,可以看成是在晶体硅的晶胞中每两个硅原子间插入一个氧原子而得到。其中硅原子的配位数为_______;己知该晶体的密度为ag/cm3,则该晶胞的棱长为______pm(用含a 、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.硫酸、纯碱、碳酸氢钠和生石灰分别属于酸、碱、盐和氧化物
B.用丁达尔效应区别FeCl3溶液和Fe(OH)3胶体
C.生石灰与水混合的过程只发生物理变化
D.H2O、CH3COOH、Cu(NH3)4SO4均含有氧,都是氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2CH3OH(g) ![]() CH3OCH3(g)+H2O(g),某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g),某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度(mol·L-1) | 0.44 | 0.6 | 0.6 |
(1)比较此时正、逆反应速率的大小:v正________v逆(填“>”、“<”或“=”)。
(2)若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH)=________;该时间内反应速率v(CH3OH)=________;CH3OH的转化率为________。
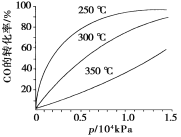
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)===CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH________0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com