
 ,空间构型三角锥形
,空间构型三角锥形分析 (1)氨气中含3对共用电子对和一对孤电子对;空间构型为三角锥形;
(2)氨气与氯化氢反应生成氯化铵固体;铵盐能和碱反应生成氨气,氨气能使润湿的红色石蕊试纸变色.
解答 解:(1)氨气中N原子最外层有5个电子,氨气中含3对共用电子对和一对孤电子对,则氨气的电子式为 ;氨气分子的空间构型为三角锥形;
;氨气分子的空间构型为三角锥形;
故答案为: ;三角锥形;
;三角锥形;
(2)氨气与氯化氢反应生成氯化铵固体,所以氨气与氯化氢气体相遇时会产生白烟,其反应的方程式为:NH3+HCl=NH4Cl;铵盐能和碱反应生成氨气,氨气能使润湿的红色石蕊试纸变蓝色,所以检验铵根离子的方法是:与碱共热,生成的气体能使湿润的红色石蕊试变蓝,说明含有铵根离子;
故答案为:生成大量白烟;NH3+HCl=NH4Cl;与碱共热,生成的气体能使湿润的红色石蕊试变蓝,说明含有铵根离子.
点评 本题考查了氨气的性质、铵根离子的检验、电子式和氨气的空间构型,题目难度不大,侧重于考查学生对基础知识的综合应用能力,注意把握铵根离子的检验方法.


科目:高中化学 来源: 题型:实验题
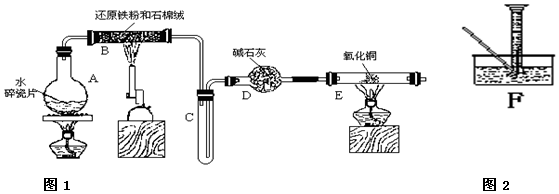
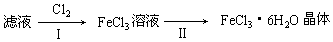
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氧化锌、硫化锌都是重要的基础化工原料.
氧化锌、硫化锌都是重要的基础化工原料.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X射线透视肠胃的内服剂--碳酸钡 | |
| B. | 熟石膏的化学化--CaSO4•2H2O | |
| C. | 工业生产氯气的原料--浓盐酸和二氧化锰 | |
| D. | 配制波尔多液原料--胆矾和石灰乳 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、H+、Cl-、NO3- | B. | Na+、Mg2+、Cl-、SO42- | ||
| C. | K+、Ba2+、OH-、I- | D. | Cu2+、H+、Br-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水能导电,所以氨水是电解质 | |
| B. | 氯化氢溶于水后能导电,但液态氯化氢不能导电 | |
| C. | 溶于水后能电离出H+的化合物都是酸 | |
| D. | 导电性强的物质一定是强电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com