
下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是①向饱和碳酸钠溶液中通入过量的CO2;②向NaAlO2溶液中逐滴加入过量的稀盐酸;③向AlCl3溶液中逐滴加入过量的稀氢氧化钠溶液;④向硅酸钠溶液中逐滴加入过量的盐酸
A.①② B.①③
C.①④ D.②③
科目:高中化学 来源: 题型:
下列推断正确的是( )
A.BF3是三角锥形分子
B.NH 的电子式:
的电子式: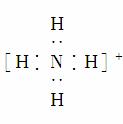 ,该离子呈平面正方形结构
,该离子呈平面正方形结构
C.CH4分子中的4个C—H键都是由氢原子的1s轨道与碳原子的p轨道形成的sp σ键
D.CH4分子中,碳原子中的sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个C—H键
查看答案和解析>>
科目:高中化学 来源: 题型:
用标准盐酸溶液滴定未知浓度的NaOH溶液(酚酞作指示剂),用“偏高”、“偏低”或“无影响”填空。
(1)酸式滴定管未用标准溶液润洗( )
(2)锥形瓶用待测溶液润洗( )
(3)锥形瓶洗净后还留有蒸馏水( )
(4)放出碱液的滴定管开始有气泡,放出液体后气泡消失( )
(5)酸式滴定管滴定前有气泡,滴定终点时气泡消失( )
(6)部分酸液滴出锥形瓶外( )
(7)酸式滴定管滴定前读数正确,滴定后俯视读数(或前仰后俯)( )
(8)酸式滴定管滴定前读数正确,滴定后仰视读数(或前俯后仰)( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.常温下,某溶液中由水电离出的c(H+)=1×10-amol·L-1,若a>7时,则该溶液的pH一定为14-a
B.pH=9的CH3COONa溶液和pH=9的NH3·H2O溶液,两溶液中水的电离程度相同
C.温度一定时,向水中滴加少量酸或碱形成稀溶液,水的离子积常数Kw不变
D.常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,将体积为Va、pH=a的某一元酸与体积为Vb、pH=b的某一元碱混合,请完成下列各题。
(1)若a+b=14,2Va=Vb,碱是NaOH,反应后所得溶液pH小于7。由此你能得到的结论是________________。
(2)若a+b=13,酸是盐酸,碱是KOH,现用盐酸滴定50.00 mL KOH溶液,当滴定到溶液的pH=2时,消耗盐酸11.11 mL。则b=________。
(3)若已知Va<Vb,a=0.5b,酸是强酸,碱是强碱,酸和碱恰好中和,则a的取值范围是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)4]2+。
回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为________________(用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式:________________________________________________________________________________________________________________________________________________。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是________________。
①硫酸铝和氢氧化钠 ②硫酸铝和氨水 ③硫酸锌和氢氧化钠 ④硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式:________________________________________________________________________________________________________________________________________________。
试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因:_____________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为探究NaHCO3、Na2CO3和盐酸(以下盐酸浓度均为1 mol·L-1)反应过程中的热效应,实验测得如下数据:
| 序号 | 35 mL试剂 | 固体 | 混合前 温度/℃ | 混合后 温度/℃ |
| ① | 水 | 2.5 g NaHCO3 | 20.0 | 18.5 |
| ② | 水 | 3.2 g Na2CO3 | 20.0 | 24.3 |
| ③ | 盐酸 | 2.5 g NaHCO3 | 20.0 | 16.2 |
| ④ | 盐酸 | 3.2 g Na2CO3 | 20.0 | 25.1 |
由此得出的结论正确的是 ( )。
A.Na2CO3溶液与盐酸的反应是吸热反应
B.NaHCO3溶液与盐酸的反应是放热反应
C.20.0 ℃时,含3.2 g Na2CO3的饱和溶液和35 mL盐酸混合后的温度将低于25.1 ℃
D.20.0 ℃时,含2.5 g NaHCO3的饱和溶液和35 mL盐酸混合后的温度将低
于16.2 ℃
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A(C11H8O4)在氢氧化钠溶液中加热反应后再酸化可得到化合物B和C。
回答下列问题:
(1)B的分子式为C2H4O2,分子中只有一个官能团。则B的结构简式是________,B与乙醇在浓硫酸催化下加热反应生成D,该反应的化学方程式是________________________________________________________________________。
该反应的类型是________;写出两种能发生银镜反应的B的同分异构体的结构简式________________________________________________________________________;
(2)C是芳香化合物,相对分子质量为180。其碳的质量分数为60.0%,氢的质量分数为4.4%,其余为氧,则C的分子式是________;
(3)已知C的芳环上有三个取代基。其中一个取代基无支链,且含有能使溴的四氯化碳溶液褪色的官能团及能与碳酸氢钠溶液反应放出气体的官能团,则该取代基上的官能团名称是________;另外两个取代基相同,分别位于该取代基的邻位和对位,则C的结构简式是________________________________________________________________________。
(4)A的结构简式是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.Na2O2可用于呼吸面具中氧气的来源
B.Na2O和Na2O2投入水中都能生成NaOH,都是氧化还原反应,它们都是碱性氧化物
C.Na2CO3可用于制玻璃、肥皂、造纸、纺织等工业,而NaHCO3可用于治疗胃酸过多、制造发酵粉等
D.NaCl的性质稳定,可用作调味品
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com