
| X | Y | ||
| Z | W |
| A、通常情况下,X元素只存在两种氧化物 |
| B、Y元素气态氢化物的还原性最强 |
| C、X元素的非金属性比Y元素非金属性强 |
| D、W的最高价氧化物对应水化物的酸性比Z的强 |


科目:高中化学 来源: 题型:
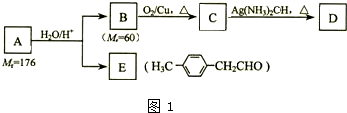 Ⅰ.已知:R-CH=CH-O-R′
Ⅰ.已知:R-CH=CH-O-R′| H2O/H+ |
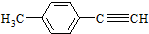 )的一条路线如图2:
)的一条路线如图2: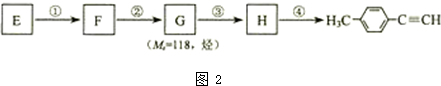
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) |
| c(HF) |
| c(H+)?c(F-) |
| c(HF) |
| A、①③④ | B、②③④ |
| C、③④⑤ | D、②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
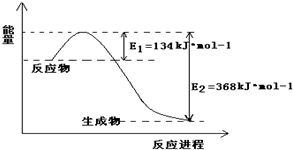 Ⅰ.(1)1molNO2和1molCO反应生成CO2和NO过程中的能量变化如图,请写出NO2和CO反应的热化学方程式
Ⅰ.(1)1molNO2和1molCO反应生成CO2和NO过程中的能量变化如图,请写出NO2和CO反应的热化学方程式查看答案和解析>>
科目:高中化学 来源: 题型:

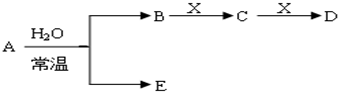
查看答案和解析>>
科目:高中化学 来源: 题型:
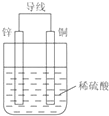 根据铜锌原电池示意图,回答下列问题:
根据铜锌原电池示意图,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该原子的摩尔质量是:aNA | ||
B、Wg该原子的物质的量是:
| ||
C、Wg该原子中含有
| ||
D、由已知信息可得:NA=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.8 gNa2O2与足量的水反应,转移的电子数为0.1NA |
| B、用含有0.1molFeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒数等于0.1NA |
| C、25℃时,pH=13的1LBa(OH)2溶液中含有的OH-数为0.2NA |
| D、100mL 12 mol?L-1浓盐酸与足量MnO2加热反应,产生的氯气分子数为0.3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com