
【题目】如图所示,下列说法正确的是( )

A. 若将乙池电解液换成 AgNO3 溶液,则可以实现在石墨棒上镀银
B. 甲池通入 CH3OH 的电极反应式为 CH3OH+6e+2H2O═CO32-+8H+
C. 反应一段时间后,向乙池中加入一定量 Cu(OH)2 固体,能使 CuSO4 溶液恢复到原浓度
D. 甲池中消耗 224mL(标准状况下)O2,此时丙池中理论上产生 1.16g 固体
【答案】D
【解析】
根据图示,甲池为原电池,通入甲醇的为负极,则乙池中银电极和丙池中右边的铂电极为阴极;通入氧气的为正极,则乙池中石墨电极和丙池中左边的铂电极为阳极,据此分析解答。
A.乙池中石墨连接甲池的正极,为电解池的阳极,银电极为阴极,若将乙池电解液换成 AgNO3 溶液,阳极上溶液中的氢氧根离子放电生成氧气,不能实现在石墨棒上镀银,故A错误;
B.在燃料电池中,负极是甲醇发生失电子的氧化反应,在碱性电解质下的电极反应为CH3OH-6e-+2H2O+8OH-=CO32-+8H2O,故B错误;
C.电解池乙池中,电解后生成硫酸、铜和氧气,要想复原,要加入氧化铜,不能加入氢氧化铜,故C错误;
D.甲池中消耗224mL(标准状况下)O2,即![]() =0.01mol,转移电子0.04mol,根据转移的电子守恒,丙池中生成0.02mol氢气,同时生成0.04mol氢氧根离子,氢氧根离子和镁离子生成氢氧化镁沉淀,所以氢氧化镁沉淀的物质的量是0.02mol,氢氧化镁沉淀的质量=0.02mol×58g/mol=1.16g,故D正确;
=0.01mol,转移电子0.04mol,根据转移的电子守恒,丙池中生成0.02mol氢气,同时生成0.04mol氢氧根离子,氢氧根离子和镁离子生成氢氧化镁沉淀,所以氢氧化镁沉淀的物质的量是0.02mol,氢氧化镁沉淀的质量=0.02mol×58g/mol=1.16g,故D正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】有机物X(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多,该化合物具有如下性质:
(1)1molX与足量的金属钠反应产生1.5 mol气体
(2)X与醇或羧酸在浓H2SO4和加热的条件下均生成有香味的产物
(3)X在一定程度下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应
根据上述信息,对X的结构判断正确的是 ( )
A.X中肯定有碳碳双键
B.X中可能有三个羟基和一个-COOR官能团
C.X中可能有三个羧基
D.X中可能有两个羧基和一个羟基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家用金属钠还原CCl4和SiCl4制得一种一维SiC纳米棒。相关反应的化学方程式为8Na+CCl4+SiCl4![]() SiC+8NaCl。下列说法不正确的是
SiC+8NaCl。下列说法不正确的是
A. 一维SiC纳米棒“比表面积”大,对微小粒子有较强的吸附能力
B. 上述反应中SiC既是氧化产物又是还原产物
C. SiCl4是由极性键构成的非极性分子
D. 每生成1 mol SiC转移8 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,有强还原性。已知:①2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑,②H3PO2+NaOH(足量)=NaH2PO2+H2O。下列推断不正确的是
A. H3PO2的结构式为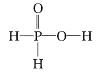
B. H3PO2具有强还原性,在空气中可能被氧化成磷酸
C. NaH2PO2是酸式盐
D. 每消耗1mol P4,反应①中转移6mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物中含有KAl(SO4)2和另外两种金属氧化物,在一定条件下可实现下图所示物质间转化:
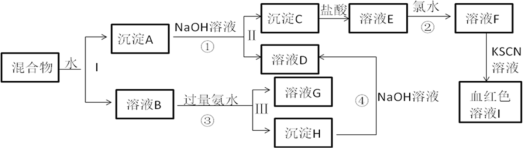
已知:Cl2+2Fe2+==2Fe3++2Cl-
请回答下列问题:
(1)沉淀H的化学式_________,框图中血红色物质是______(填化学式)
(2)Ⅰ、Ⅱ、Ⅲ分离操作中所需的玻璃仪器除烧杯、玻璃棒外还需要___________。
(3)反应①的离子方程式是____________。
(4)检验溶液G中金属阳离子的操作方法和现象是___________。
(5)若在E中加入KSCN溶液,溶液不变色,则沉淀C是________(填名称);
若在E中加入KSCN溶液,溶液变红色,为进一步确认沉淀C的成分,进行如下定量实验: 将沉淀C用5mol/L盐酸14mL恰好完全溶解,所得溶液还能吸收标准状况下56mL氯气,使其中Fe2+全部转化为Fe3+。则沉淀C可能的化学式是__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错误的是
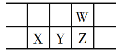
A. 原子半径:W<X
B. 常温常压下,Y单质为固态
C. 气态氢化物热稳定性:Z<W
D. X的最高价氧化物的水化物是强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液X含有H+、Al3+、NH4+、Fe2+、Fe3+、HCO3-、S2-、SO42-、Cl-、OH-中的一种或几种,取该溶液进行实验,实验内容和相关数据(气体体积在标准状况下测定)如下:
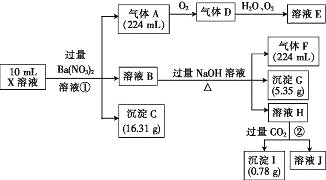
(1)通过上述实验过程,一定不存在的离子是_______。
(2)反应①中生成A的离子方程式为________。
(3)若测得X溶液中c(H+)=6mol·L-1,则X溶液中_______(填“含”或“不含”)Fe3+,c(Fe3+)=________mol·L-1(若填不含,则不需计算),X溶液中c(Cl-)=_______mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列短周期元素性质的数据,回答下列问题:

(1)元素③在周期表中位置是__;元素④与元素⑦相比较,气态氢化物较稳定的是__(填化学式);
(2)元素①是__(写元素符号),元素⑥是__(写元素符号),二者按照原子个数比为1∶1形成的化合物与水反应的化学方程式为:___。
(3)元素⑤与元素②的非金属性强弱顺序为__(写元素符号),元素⑤的单质通入到元素②的氢化物的水溶液中,反应的化学方程式为:___。
(4)用电子式表示元素①氢化物的形成过程___。写出元素⑦氢化物的电子式__;写出实验室制元素⑤单质的化学反应方程式__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、环境密切相关。下列说法正确的是
A. 明矾在水中生成的![]() 胶体有吸附性,因此常用明矾对水进行消毒
胶体有吸附性,因此常用明矾对水进行消毒
B. 因汽油不完全燃烧使汽车尾气中含有少量氮氧化物
C. 液氨汽化吸收大量热,所以液氨常用作制冷剂
D. Al(OH)3具有很高的熔点,是优良的耐高温材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com