
 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平 衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
分析 (1)相同条件下,酸的电离平衡常数越小,则酸的电离程度越小,酸根离子水解程度越大,则相同浓度的钠盐,其pH值越大;
(2)加水稀释促进醋酸电离,溶液中氢离子浓度、醋酸分子浓度、醋酸根离子浓度都减小,温度不变水的离子积常数不变,氢氧根离子浓度增大;
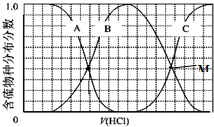
(3)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸,盐酸和氢氧化钠先反应,然后和硫化钠反应,结合图1所示H2S、HS-、S2-的分布分数进行解答;NaHS的含量先增加后减少;根据物料守恒可求得滴加过程中,溶液中微粒浓度大小关系;根据电离平衡和水解规律可得M点时,溶液中反应.
解答 解:(1)相同条件下,酸的电离平衡常数越小,则酸的电离程度越小,酸根离子水解程度越大,则相同浓度的钠盐,其pH值越大,根据电离平衡常数知,酸根离子水解程度大小顺序是:CO32->ClO->HCO3->CH3COO-,所以这几种盐的pH大小顺序是a<d<c<b,
故答案为:a<d<c<b;
(2)A.加水稀释促进醋酸电离,但溶液中c(H+)减小,故错误;
B.加水稀释促进醋酸电离,所以氢离子个数增大,醋酸分子个数减小,则$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ 增大,故正确;
C.温度不变,则c(H+)•c(OH-)不变,故错误;
D.加水稀释促进醋酸电离,但溶液中氢离子浓度减小,温度不变,水的离子积常数不变,氢氧根离子浓度增大,所以$\frac{c(O{H}^{-})}{c({H}^{+})}$增大,故正确;
E.温度不变,电离平衡常数不变,则$\frac{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$不变,故错误;
故选BD;
(3)①向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸,盐酸和氢氧化钠先反应,然后和硫化钠反应,A表示含硫微粒浓度减小为S2-,B先增加后减少为HS-,C浓度一直在增加为H2S,向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸,因体积相同,设Na2S、NaOH各为1mol,则n(Na)=3n(S),溶液中含硫的微粒为HS-、S2-、H2S,则c(Na+)=3[c(H2S)+c(HS-)+c(S2-)],或溶液中存在电荷守恒得到c(Na+)=c(Cl-)+c(OH-)+c(HS-)+2c(S2-)-c(H+);
故答案为:HS-;3[c(H2S)+c(HS-)+c(S2-)]或c(Cl-)+c(OH-)+c(HS-)+2c(S2-)-c(H+);
②B为HS-,C表示H2S,当滴加盐酸至M点时,表示两者含量相等,随盐酸滴加发生的反应为:HS-+H+=H2S,则反应的离子方程式为:2S2-+3H+=HS-+H2S;
故答案为:2S2-+3H+=HS-+H2S.
点评 本题考查了弱电解质的电离,明确弱电解质的电离特点、电离平衡常数与酸根离子水解程度的关系再结合守恒思想分析解答,难度中等.


科目:高中化学 来源: 题型:多选题
| A. | 分别与足量盐酸反应时①消耗盐酸量少 | |
| B. | 分别与足量氯化钡溶液反应时①产生的沉淀多 | |
| C. | 分别配成等体积的溶液时②的c(Na+)大 | |
| D. | 相同条件下,分别与足量盐酸反应时放出的CO2体积相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中加少量NaOH | B. | 向水中加少量AlCl3 | ||
| C. | 向水中加少量H2SO4 | D. | 向水中加入少量NaC |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
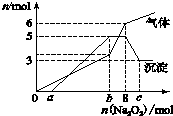 1.某废水中可能含有下列离子中的若干种:Fe3+、Al3+、Fe2+、Cu2+、Cl-、CO32-、NO3-、SO42-、SiO32-.现进行如下实验:
1.某废水中可能含有下列离子中的若干种:Fe3+、Al3+、Fe2+、Cu2+、Cl-、CO32-、NO3-、SO42-、SiO32-.现进行如下实验:| 阳离子 | H+、K+、Al3+、NH4+、Mg2+ |
| 阴离子 | Cl-、Br-、OH-、CO32-、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 固体中阳离子和阴离子个数不一定相等 | |
| B. | 固体中一定有离子键可能有共价键 | |
| C. | 若X只含两种元素,所含元素一定不在同一周期也不在同一主族 | |
| D. | 固体中阳离子半径一定大于阴离子半径 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
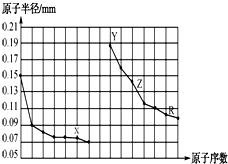
| A. | 同周期非金属元素中,X氢化物的沸点最高 | |
| B. | Y、Z的单质在空气中加热,均可发生燃烧反应 | |
| C. | Y、Z、R对应的最高价氧化物的水化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
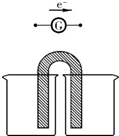 化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养.
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期\族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
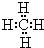 ,写出该化合物跟⑧的单质发生置换反应的化学方程式:CH4+2Cl2 $\frac{\underline{\;一定条件\;}}{\;}$C+4HCl.
,写出该化合物跟⑧的单质发生置换反应的化学方程式:CH4+2Cl2 $\frac{\underline{\;一定条件\;}}{\;}$C+4HCl.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com