
【题目】下列化学反应中,属于氧化还原反应的是
A. SO3+H2O=H2SO4 B. CaCO3![]() CaO+CO2↑
CaO+CO2↑
C. Zn+H2SO4=ZnSO4+H2↑ D. AgNO3+HCl=AgCl↓+HNO3
【答案】C
【解析】A项,反应前后S元素、H元素、O元素的化合价都分别为+6价、+1价、-2价,反应前后元素化合价没有升降,不是氧化还原反应;B项,反应前后Ca元素、C元素、O元素的化合价都分别为+2价、+4价、-2价,反应前后元素化合价没有升降,不是氧化还原反应;C项,Zn元素的化合价由0价升至ZnSO4中+2价,H元素的化合价由H2SO4中+1价降至H2中0价,反应前后元素化合价有升降,属于氧化还原反应;D项,反应前后Ag元素、N元素、O元素、H元素、Cl元素的化合价都分别为+1价、+5价、-2价、+1价、-1价,反应前后元素化合价没有升降,不是氧化还原反应;属于氧化还原反应的是C,答案选C。


科目:高中化学 来源: 题型:
【题目】铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:
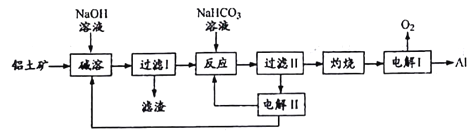
注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为____________。
(2)向“过滤I”所得滤液中加入NaHCO3溶液,溶液的PH_____(填“增大”、“不变”或“减小”),NaHCO3中存在化学键有______
(3)“电解I”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是________。
(4)“电解II”是电解Na2CO3溶液,原理如图所示。

阳极的电极反应式为_______,阴极产生的物质A的化学式为_______。
(5)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为海水利用的部分过程。下列有关说法正确的是
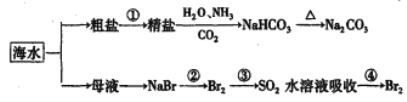
A. 粗盐提取精盐的过程只发生物理变化
B. 用澄清的石灰水可鉴别Na2CO3产品是否含有NaHCO3
C. 在第②、④步骤中,溴元素均被还原
D. 制取NaHCO3的反应是利用其溶解度小于NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示A、B、C、D、E的变化关系,回答下列问题:
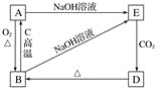
(1)写出A、D的名称:A__________,D__________。
(2)写出B→A的化学方程式:______________。
(3)写出下列反应的离子方程式:
A→E:__________________________________;B→E:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X,Y均为1~18号之间的元素,X,Y可形成化合物X2Y和X2Y2 , 又知Y的原子序数小于X的原子序数,则两种元素的原子序数之和为( )
A.19
B.18
C.27
D.9
查看答案和解析>>
科目:高中化学 来源: 题型:
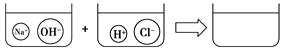
【题目】复分解反应能够发生是因为在这些反应物中含有一些“特殊”的阴、阳离子,它们能相互结合。如反应“BaCl2+Na2SO4![]() BaSO4↓+2NaCl”中,实际参加反应的离子是Ba2+和SO42-,而Cl、Na+则是“旁观者”,并没有参加反应。请你反应“K2CO3+2HCl=2KCl+CO2↑+H2O”中实际参加反应的离子是________;该反应的离子方程式是____________________________。请根据你的想象,在下图右边的容器中画出体现NaOH溶液和稀盐酸反应产物的示意图。
BaSO4↓+2NaCl”中,实际参加反应的离子是Ba2+和SO42-,而Cl、Na+则是“旁观者”,并没有参加反应。请你反应“K2CO3+2HCl=2KCl+CO2↑+H2O”中实际参加反应的离子是________;该反应的离子方程式是____________________________。请根据你的想象,在下图右边的容器中画出体现NaOH溶液和稀盐酸反应产物的示意图。
 ________
________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列数据:4Al(s)+3O2(g)=2Al2O3(s) △H=-3350kJ·mol-1
2Fe(s)+O2(g)=2FeO(s) △H=-544kJ·mol-1
则2Al(s) +3FeO(s)=Al2O3(s) + 3Fe(s)的△H是( )
A. +1403 kJ·mol-1 B. -859 kJ·mol-1
C. -1718 kJ·mol-1 D. -2806kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. NO2通入水中:3NO2+H2O=2H++2NO2-+NO
B. Fe(OH)3溶于HI溶液:Fe(OH)3+3H+=Fe3++3H2O
C. (NH4)2SO4溶液中加入Ba(OH)2溶液:NH4++SO42-+Ba2++OH-=BaSO4↓+NH3·H2O
D. 向NaAlO2溶液中滴入NaHCO3溶液产生白色沉淀:AlO2-+HCO3-+H2O=Al(OH)3↓+CO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.尿素[CO(NH2)2]是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为两步反应:
第一步:2NH3(g)+CO2(g)===H2NCOONH4(s) ΔH=-272kJ·mol-1
第二步:H2NCOONH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+138kJ·mol-1
(1)写出工业上以NH3、CO2为原料合成尿素的热化学方程式:_________________________
(2)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如下图所示:
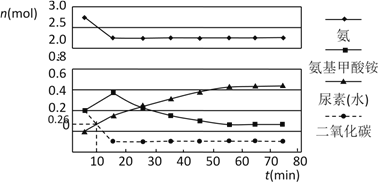
已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第_________步反应决定,总反应进行到_________min时到达平衡。
(3)电解尿素[CO(NH2)2]的碱性溶液制纯净氢气的过程中同时产生氮气。电解时,阳极的电极反应式为________________________________。
Ⅱ.用焦炭还原NO2的反应为:2NO2(g)+2C(s )![]() N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
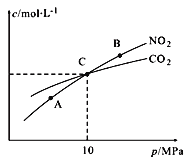
①A、B两点的浓度平衡常数关系:Kc(A)_______Kc(B) (填 “﹥”、“<”或“﹦”)。
②计算C点时该反应的压强平衡常数Kp(C)=______(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com