
己知:
(1)Al(OH)3的电离方程式:AlO2-+H++H2O Al(OH)3
Al(OH)3 A13++3OH-
A13++3OH-
(2)无水AlCl3晶体的沸点:182.9℃,溶于水的电离方程式为:AlCl3=Al3++3Cl-
(3)PbSO4难溶于水,易溶于醋酸钠溶液,反应的化学方程式为:PbSO4+2CH3COONa=Na2SO4+(CH3COO)2Pb
则下列关于A1(OH)3、AlCl3和(CH3COO)2Pb的说法中正确的是( )
A.均为强电解质 B.均为弱电解质
C.均为离子化合物 D.均为共价化合物
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:选择题
某烃的一种同分异构体只能生成一种一氯代物,该烃的分子式可以是
A.C3H8 B.C4H10 C.C5H12 D.C6H14
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高一上期中化学试卷(解析版) 题型:选择题
下列离子方程式中,书写正确的是( )
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3 H2O Fe(OH)3↓+3 H+
Fe(OH)3↓+3 H+
B.澄清石灰水与稀盐酸反应Ca(OH)2 + 2 H+ ═ Ca2+ + 2 H2O
C.稀硫酸除铁锈:Fe2O3 + 6 H+ == 2 Fe3+ + 3 H2O
D.硫酸和Ba(OH)2反应: Ba2+ + OH- + SO42- + H+ = BaSO4↓ + H2O
查看答案和解析>>
科目:高中化学 来源:2017届河南省周口市高三上10月月考化学试卷(解析版) 题型:推断题
X、Y、Z、W四种物质有如下相互转化关系(其中各X、W为单质,Y、Z为化合物,未列出反应条件)。

Ⅰ.若Z是生活中常用的调味品,W遇淀粉溶液变蓝,则:
工业上Z有多种用途,用化学方程式表示Z的一种用途:________________。
生活中所用的Z加入了碘酸钾,过量X与Y溶液反应时可以得到一种碘酸盐,此反应的离子方程式是________________。
Ⅱ.若X是工业上用量最大的金属单质,Z是一种具有磁性的黑色晶体,则:
(1)X与Y反应的化学方程式是________________。
(2)若用下列装置只进行Z+W→X+Y反应(夹持装置未画出);

①完成此实验有多步操作,其中三步是:
A.点燃酒精灯 B.滴加盐酸 C.检验气体纯度
这三步操作的先后顺序是 (填字母)。
②为保证实验成功,上述装置需要改进,方法是(用文字叙述) 。
(3)将3.38gZ加入50ml4mol/L 稀HNO3中充分反应,产生112ml的NO(标准状况),向反应后的溶液中滴加NaOH溶液能产生沉淀。当沉淀量最多时,至少需要加入2mol/L的NaOH溶液__________ml.(精确到0.1)。
查看答案和解析>>
科目:高中化学 来源:2017届河南省周口市高三上10月月考化学试卷(解析版) 题型:选择题
海水是重要的资源,可以制备一系列物质,
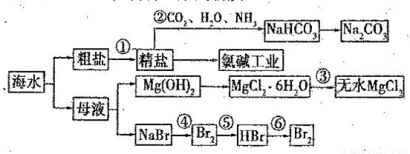
下列说法正确的是( )
A.步骤②中,应先通CO2 ,再通NH3
B.步骤③可将MgCl2·6H2O晶体在空气中直接加热脱水
C.步骤④、⑤、⑥反应中,溴元素均被氧化
D.除去粗盐中的 SO42-、Ca2+ 、Mg2+ 等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2 溶液→Na2CO3 溶液→过滤→盐酸
查看答案和解析>>
科目:高中化学 来源:2017届河南省周口市高三上10月月考化学试卷(解析版) 题型:选择题
下列有关实验的现象描述正确的是
A.氢气在氯气中燃烧,火焰呈淡蓝色,瓶口出现大量暈白雾
B.将新制的氯气通入AgNO3溶液中,白色沉淀生成.
C.铜在氯气中燃烧,产生大量棕色的烟,加水溶解后可得蓝绿色溶液
D.用洁净的铂丝沾取碳酸钾粉末在酒精灯火焰上灼烧,可观察到明亮的紫色火焰
查看答案和解析>>
科目:高中化学 来源:2017届广西省柳州市高三10月模拟理综化学试卷(解析版) 题型:填空题
用含有Al2O3、SiO2和少量FeO•xFe2O3的铝灰制备Al2(SO4)3•18H2O,工艺流程如下:

(一定条件下,MnO4-可与Mn2+反应生成MnO2)
已知:生成氢氧化物沉淀的PH

(1)H2SO4溶解Al2O3的离子方程式是____________。
(2)检验滤液中还存在Fe2+的方法是______________。
(3)“除杂”环节有如下几个步骤:(I)向滤液中加入过量KMnO4溶液,调节溶液的pH为3.2 (II)加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;(Ⅲ)加入MnSO4至紫红色消失,过滤。
①步骤I 的目的是:_________;调节溶液的pH为3.2的目的是__________。
②向步骤II的沉淀中加入浓HCl并加热,有黄绿色气体生成,写出其反应方程式______。
③步骤Ⅲ中加入MnSO4的目的是__________(用离子反应方程式表示)
(4)从多次循环使用后母液中可回收的主要物质是________(填化学式)。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省安庆市等六校高三第一次联考化学试卷(解析版) 题型:选择题
二茂铁[(C5H5)2Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域。已知二茂铁熔点是173 ℃(在100 ℃时开始升华),沸点是249 ℃,不溶于水,易溶于苯、乙醚等非极性溶剂。下列说法不正确的是( )
A.二茂铁属于分子晶体
B.在二茂铁结构中,C5H 与Fe2+之间形成的化学键类型是离子键
与Fe2+之间形成的化学键类型是离子键
C.已知:环戊二烯的结构式为: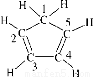 ,则其中仅有1个碳原子采取sp3杂化
,则其中仅有1个碳原子采取sp3杂化
D.C5H 中一定含π键
中一定含π键
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨师大附中高二上期中化学卷(解析版) 题型:计算题
温度为T时,在4.0 L恒容密闭容器中充入2.0 mol PCl5,发生反应:
PCl5(g) PCl3(g)+Cl2(g),反应时间(t)与容器内气体总压强(p)的数据见下表:
PCl3(g)+Cl2(g),反应时间(t)与容器内气体总压强(p)的数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
总压强p/100kPa | 100 | 116 | 119 | 120 | 120 |
(1)由总压强p和起始压强p0计算反应物PCl5的转化率α(PCl5)的表达式为?平衡时PCl5的转化率为多少?
(2)反应在前50 s的平均速率v(PCl3)为多少?
(3)该温度下 的平衡常数为多少?
的平衡常数为多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com