
| ||
| ||
| ||
| ||


 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案科目:高中化学 来源: 题型:
| A、AgCl不溶于水,不能转化为AgI | ||||
| B、在含浓度均为0.001mol?L-1的Cl-、I-的溶液中缓慢滴AgNO3稀溶液,先析出AgI | ||||
| C、AgI比AgCl更难溶于水,所以AgCl可转化为AgI | ||||
D、常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于
|
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
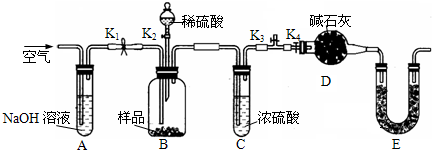
查看答案和解析>>
科目:高中化学 来源: 题型:

| 1 |
| 2 |
| c(H2) |
| c(CH3OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、46g NO2含有NA个NO2分子 |
| B、10L pH=1的硫酸溶液中含有的H+离子数为2NA |
| C、标准状况下,NA个CO2分子所占的体积约为22.4 L |
| D、1mol Al3+离子含有的核外电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu(OH)2>CuCO3>CuS |
| B、CuS>Cu(OH)2>CuCO3 |
| C、CuS<Cu(OH)2<CuCO3 |
| D、Cu(OH)2<CuCO3<CuS |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升温至30℃ |
| B、降温 |
| C、加入NaOH溶液 |
| D、加入稀HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2分子的结构式:O-C-O | ||
B、Na+的结构示意图: | ||
C、NH3分子的电子式: | ||
D、质量数为18的氧原子:
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com