
某无色透明溶液中存在大量的H+、Cl一、NO3一,该溶液中还可能大量存在的是
A.HCO3一 B.NH4+ C.Cu2+ D.Ag+
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:
313 K时,水的KW=3.0×10-14,则在313 K时,c(H+)=1.0×10-7 mol·L-1的溶液( )
A.呈酸性 B. 呈中性
呈中性
C.呈碱性 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
有四种物质的量浓度相等、且都由一价阳离子A+和B+及一价阴离子X-和Y-组成的盐溶液。据测定常温下AX和BY溶液的pH=7,AY溶液的pH>7,BX溶液的pH<7,由此判断不水解的盐是( )
A.BX B.AX
C.AY D.BY
查看答案和解析>>
科目:高中化学 来源: 题型:
生活离不开化学,下列做法不合适的是
A.用白醋清洗热水瓶中的水垢
B.用灼烧并闻气味的方法区别纯棉织物和纯羊毛织物
C.用铝锅长时间存放剩菜
D.利用激光笔区别鸡蛋白溶液和浓盐水
查看答案和解析>>
科目:高中化学 来源: 题型:
蛇纹石矿由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁实验步骤如下:
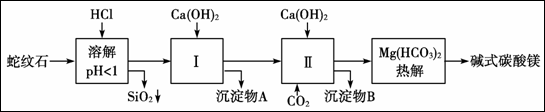
已知:
| 氢氧化物 | Fe(OH) 3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
(1)蛇纹石加盐酸溶解后,溶液里除了Mg2+外,还含有的阳离子有 。
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见上表),Ca(OH)2不能过量,若Ca(OH)2过量可能会导致 溶解、 沉淀。
(3)物质循环使用,能节约资上述实验中,可以循环使用的物质是 。
(4)高温煅烧碱式碳酸镁aMgCO3·bMg(OH)2·cH2O得到MgO。取碱式碳酸镁4.66 g,高温煅烧至恒重,得到固体2.00 g和标准状况下CO2 0.896 L,通过计算确定碱式碳酸镁的化学式为 。(写出计算过程,否则不得分)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16。下列关于难溶物之间转化的说法中错误的是( )
A.AgCl不溶于水,不能转化为AgI
B.两种难溶物的Ksp相差越大,难溶物就越容易转化为更难溶的物质
C.AgI比AgCl更难溶于水,所以AgCl可以转化为AgI
D.常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于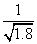 ×10-11 mol·L-1
×10-11 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
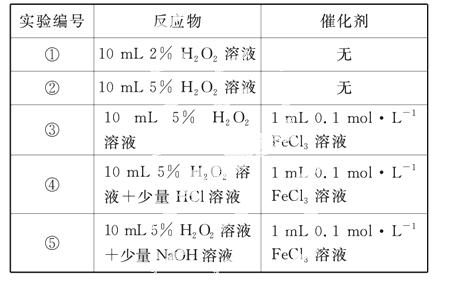
(1)催化剂能加快化学反应速率的原因是____________。
(2)实验①和②的目的是___________________。
实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是__________。
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。
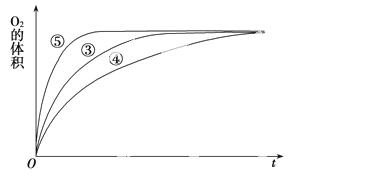
分析上图能够得出的实验结论是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com