
【题目】下列说法正确的是( )
A. 氧化还原反应的本质是元素化合价发生变化
B. 还原剂是一种能够得到电子的物质
C. 物质所含元素化合价升高的反应是还原反应
D. 氧化反应和还原反应是同时发生的
 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
【题目】在电解质溶液中,下列叙述正确的是( )
A. 阳离子和阴离子数目一定相等
B. 阳离子带的正电荷总数一定和阴离子带的负电荷总数相等
C. 除阴、阳离子外,溶液中不会再有其他粒子
D. 电解质溶液的导电性一定很强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2mol有机物和0.4mol O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g).产物经过浓硫酸后,浓硫酸的质量增加10.8g;再通过灼热CuO充分反应后,固体质量减轻3.2g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6g.0.1mol该有机物恰好与4.6g金属钠完全反应.下列关于该有机物的说法不正确的是( )
A.该化合物的相对分子质量是62
B.该化合物的化学式为C2H6O2
C.1 mol该化合物能与2 mol O2发生催化氧化反应
D.1 mol该有机物最多能与2 mol Na反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有①汽车;②机器上的齿轮;③门把手;④锯条;⑤铁制洗脸盆等常见铁制品。为了防止它们生锈,通常适合采用下面哪一种方法。(填序号)
(1)在表面喷漆;
(2)在表面涂油;
(3)在表面镀一层其他金属;
(4)在表面烧制搪瓷;
(5)使其表面形成致密的氧化物保护膜。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关仪器用法正确的是( )
A.对试管进行加热一定不能使用石棉网
B.使用滴定管量取液体,可精确至0.01mL
C.用量筒量取一定体积的溶液,要洗涤2~3次,确保溶液全部转移
D.酸碱滴定实验中,锥形瓶干燥后使用可减少误差
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学社两位同学为探究铜跟浓硫酸的反应,设计了图所示装置. 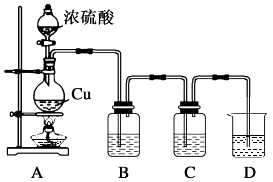
(1)反应开始前必须进行的操作是 .
(2)装置A中发生的反应的化学方程式为 .
(3)洗气瓶B中为品红溶液,确认有SO2生成的现象是 .
(4)洗气瓶C中为新制的氯水,反应的现象是新制氯水由淡黄绿色变为 , 原因是SO2具有性.
(5)烧杯D中盛装的试剂是浓度较大的溶液,其作用是
(6)若反应中有2mol电子转移,则生成的SO2在标准状况下的体积是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关。下列说法正确的是
A.生石灰、铁粉、硅胶是食品包装中常用的干燥剂
B.乙醇溶液、双氧水均可用于杀菌消毒,但原理不同
C.纯碱是焙制糕点所用发酵粉的主要成分之一
D.SiO2具有导电性,可用于制造光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
(1)![]() 系统命名法为 ,
系统命名法为 ,
(2)4﹣甲基﹣1﹣戊烯的键线式为 ,
(3)写出乙醛与新制氢氧化铜反应化学方程式 ,
(4)下列有关实验的说法不正确的是 . A.制乙烯时,温度计应插入反应混合液中
B.检验C2H5Cl中氯元素时,将C2H5Cl和NaOH水溶液混合加热,然后用稀硫酸酸化,再加入AgNO3溶液
C.做过银镜反应的试管用氨水洗涤,做过苯酚的试管用酒精洗涤
D.将一定量CuSO4和NaOH溶液混合后加入甲醛溶液,加热未产生砖红色沉淀,原因可能是NaOH量太少.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前“低碳减排”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题.
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g)2CO2(g)+N2(g).在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂表面积(S)和时间(I)的变化曲线如图所示.据此判断:
①该反应的△H0(填“>”或“<”).
②在T2温度下,0﹣2s内的平均反应速率v(N2)=mol/(Ls).
③若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是(填代号).
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
例如:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=﹣867kJmol﹣1
2NO2(g)═N2O4(g)△H=﹣56.9kJmol﹣1
写出CH4(g)催化还原N2O4(g)的热化学方程式: .
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的.如图是通过人工光合作用,以CO2(g)和H2O(g)为原料制备HCOOH和O2的原理示意图.催化剂b表面发生的电极反应为 . 
③常温下0.1molL﹣1的HCOONa溶液pH为10,则HCOOH的电离常数Ka=molL﹣1(填写最终计算结果).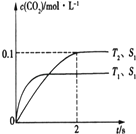
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com