
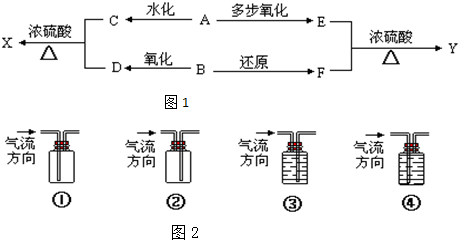
分析 A的密度在标准状况下为1.25g/L,所以A的相对分子质量为1.25×22.4=28;A、B、X、Y的分子式都符合CnH2nO0.5n-1,所以A的分子式为C2H4,所以A为乙烯(CH2=CH2),A多步氧化得E为CH3COOH,A水化得C为CH3CH2OH,F和C互为同系物,所以F为醇类,B还原得到F,说明B为醛类物质,B中含支链,且核磁共振氢谱测得有3个吸收峰,峰高6:1:1,可推知B为(CH3)2CHCHO,则D为(CH3)2CHCOOH,F为(CH3)2CHCH2OH,根据图中的转化可知,X为(CH3)2CHCOOCH2CH3,Y为CH3COOCH2CH(CH3)2,以此解答该题.
解答 解:A的密度在标准状况下为1.25g/L,所以A的相对分子质量为1.25×22.4=28;A、B、X、Y的分子式都符合CnH2nO0.5n-1,所以A的分子式为C2H4,所以A为乙烯(CH2=CH2),A多步氧化得E为CH3COOH,A水化得C为CH3CH2OH,F和C互为同系物,所以F为醇类,B还原得到F,说明B为醛类物质,B中含支链,且核磁共振氢谱测得有3个吸收峰,峰高6:1:1,可推知B为(CH3)2CHCHO,则D为(CH3)2CHCOOH,F为(CH3)2CHCH2OH,根据图中的转化可知,X为(CH3)2CHCOOCH2CH3,Y为CH3COOCH2CH(CH3)2,
(1)由以上分析可知B的结构简式为 (CH3)2CHCHO,Y的结构简式为CH3COOCH2CH(CH3)2,
故答案为:(CH3)2CHCHO;CH3COOCH2CH(CH3)2;
(2)C和D生成X是酯化反应,也是取代反应,故答案为:CD;
(3)实验室制取CH2=CH2的化学反应方程式为CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,
故答案为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;
(4)实验室组装A的发生装置时,用到的玻璃仪器除酒精灯和导气管外,还有圆底烧瓶、温度计,故答案为:烧瓶、温度计;
(5)乙烯密度和空气接近,不溶于水,可用排水法收集,③符合要求,故答案为:③;
(6)实验室制取A时,常因温度过高而生成有刺激性气味的气体二氧化硫,由于二氧化硫也有还原性,所以在检验乙烯的还原性时必须先除去二氧化硫,要以用亚硫酸钠溶液吸收二氧化硫,还要用品红检验二氧化硫是否被除尽,再用高锰酸钾检验乙烯的还原性即可,用无水硫酸铜先检验水,最后用澄清石灰水检验二氧化碳,故所选试剂的顺序为④⑤①③②,
故答案为:B.
点评 本题考查了有机物结构简式的推断和有机合成路线的分析,为高考常见题型,题目难度中等,准确把握有机官能团之间的转化是解题的关键,侧重于考查学生分析问题的能力,难点是同分异构体种类的判断,解题的关键是A、B物质的确定,答题时注意有机基础知识的灵活运用.


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 定容时,眼睛仰视刻度线 | |
| B. | 反复倒转摇匀后,液面低于刻度线,再加蒸馏水至液面最低点恰好与刻度线相平 | |
| C. | 洗涤烧杯和玻璃棒的溶液未转移入容量瓶中 | |
| D. | 溶解后的溶液未冷却至室温就转移入容量瓶中并定容 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | A-A | B=B | A-B |
| 键能kJ/mol | 236 | 406 | 163 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 75 mL 2 mol/L的CaCl2 | B. | 100 mL 2 mol/L的NH4Cl | ||
| C. | 150 mL 1mol/L的KCl | D. | 100 mL 3 mol/L的NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO | CO2 | 通入足量的氢氧化钠溶液,干燥 |
| B | NaCl | 泥沙 | 加入足量的水溶解、过滤、蒸发 |
| C | NaOH溶液 | Na2CO3 | 加入足量的稀盐酸至不再产生气泡 |
| D | FeCl2溶液 | CuCl2 | 加入过量的铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 气体Y是SO2和H2的混合物 | B. | 气体Y中SO2和H2的体积比为4:1 | ||
| C. | 反应中共消耗锌87.5g | D. | 反应中共转移电子3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
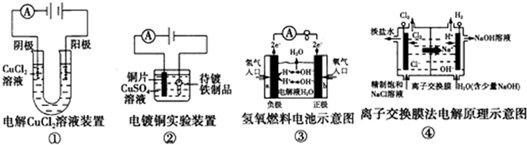
| A. | ①装置中阴极处产生的气体能够使湿润的淀粉KI试纸变蓝 | |
| B. | ②装置不能完成在铁制品上镀铜 | |
| C. | ③装置中电子由b极流向a极 | |
| D. | ④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上第二次适应性考试化学卷(解析版) 题型:推断题
某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。
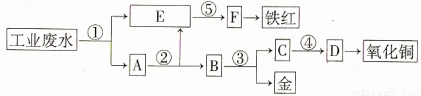
填写下面空白。
(1)图中标号处需加入的相应物质分别是① 、② 、③ 、④ 、⑤ ;
(2)写出①处发生反应的离子方程式 ;写出③处发生反应的化学方程式 ;
(3)铁红的化学式为 ;分别写出铁红和氧化铜在工业上的一种主要用途:铁红 ;氧化铜 。
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
捕碳技术是指从空气中捕获CO2的技术。目前NH3已经被用作工业捕碳剂。下列物质中不能作为捕碳剂的是
A.Na2CO3 B.H2NCH2CH2NH2 C.(NH4)2CO3 D.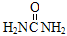
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com