
亚硝酸钠被称为工业盐,在漂白、电镀等方面应用广泛。以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示(部分夹持装置略)。
已知:室温下,①2NO+Na2O2→2NaNO2 ②3NaNO2+3HCl→3NaCl+HNO3+2NO↑+H2O;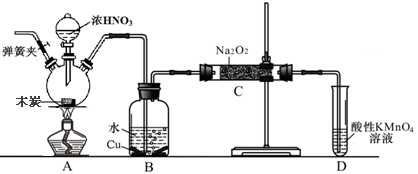
③酸性条件下,NO或NO2–都能与MnO4–反应生成NO3–和Mn2+
完成下列填空:
(1)写出浓硝酸与木炭反应的化学方程式 。
(2)B中观察到的主要现象是 ,D装置的作用是 。
(3)检验C中产物有亚硝酸钠的方法是 。
(4)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和 ,为避免产生这些副产物应在B、C装置间增加装置E,画出E并注明E中盛放的药品名称 。
(5)写出检验C产物中是否含碳酸钠的方法 。
(6)将1.56g过氧化钠完全转化成为亚硝酸钠,理论上至少需要木炭 g。
(1)C+4HNO3(浓)=加热=CO2+4NO2+2H2O
(2)铜片逐渐溶解,溶液变为蓝色,有无色气体产生 吸收未反应的NO
(3)取样,加入稀盐酸,产生无色气体,遇到空气变为红棕色
(4)氢氧化钠 干燥管 碱石灰
(5)取样,加入酸性高锰酸钾溶液,若有使澄清石灰水变浑浊的气体产生,则有碳酸钠
(6)0.36g(关系式法C~4NO2~4/3 NO~2/3 Na2O2 )
解析试题分析:(1)写出浓硝酸与木炭在加热条件下发生氧化还原反应的化学方程式C+4HNO3(浓)=加热=CO2+4NO2+2H2O。
(2)A中生成的二氧化氮进入B中并与水反应,生成了硝酸,硝酸和铜反应,观察到的主要现象是铜片逐渐溶解,溶液变为蓝色,有无色气体产生,由于一氧化氮有毒,D装置的作用是吸收未反应的NO。
(3)检验C中产物有亚硝酸钠的方法是取样,加入稀盐酸,产生无色气体,遇到空气变为红棕色。
(4)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和氢氧化钠,氢氧化钠是由水和过氧化钠生成,为避免产生这些副产物应在B、C装置间增加干燥装置E,药品名称碱石灰放在干燥管中。
(5)检验碳酸根的方法:取样,加入酸性高锰酸钾溶液,若有使澄清石灰水变浑浊的气体产生,则有碳酸钠。
(6)将1.56g过氧化钠是0.02mol,完全转化成为亚硝酸钠,根据①2NO+Na2O2→2NaNO2,生成NaNO2 0.04mol,C+4HNO3(浓)=CO2+4NO2+2H2O,3NO2+2H2O=2HNO3 + NO +H2O,得出关系式1.5C---2NaNO2,可求得碳的物质的量为0.03mol,理论上至少需要木炭0.36g。
考点:本题主要考查由性质推断实验现象和多步骤反应中的化学计算。


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:实验题
发酵粉是一种化学膨松剂,可由小苏打、臭粉(碳酸氢铵)、明矾中的两种物质组成。某小组为探究不同品牌的发酵粉的化学成分,进行如下实验。
【提出假设】
(1)假设1:由小苏打和臭粉组成
假设2:由小苏打和明矾组成
假设3:由 组成
【方案与流程】
为探究甲品牌的发酵粉的成分,某同学设计如下实验,得到如下现象: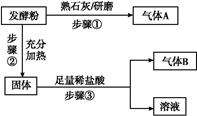
(2)结合步骤①~③分析,气体A为 ,该发酵粉的成分为 (填化学式)。
(3)若步骤①和②操作不变(现象也相同),将步骤③中足量稀盐酸改为足量氯化钡溶液,观察到有白色沉淀生成,能否确定发酵粉的成分并说明理由: 。
(4)乙品牌的发酵粉的化学组成可能为假设2情况,请你设计实验验证。
实验仪器和用品任选,限选试剂:稀盐酸、0.1 mol/L NaOH溶液
写出实验步骤、预期现象和结论。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量样品溶于足量的盐酸后,将溶液分成两份,分别装入A、B试管中 | |
| 步骤2: | ,证明有Na+,发酵粉中有NaHCO3 |
| 步骤3: | ,结合步骤2中的结论,假设2成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
乙二酸(H2C2O4)俗称草酸,是一种重要的化工原料。查阅资料,了解到以下有关信息:
①乙二酸易溶于水,加热至100℃开始升华,125℃时迅速升华,157℃时大量升华并开始分解。乙二酸受热分解生成水、二氧化碳和一种常见的还原性气体。
②乙二酸的钙盐——乙二酸钙为不溶于水的白色晶体。
(1)请写出乙二酸受热分解的化学方程式______________________。
(2)化学兴趣小组的同学用实验证明乙二酸晶体受热分解生成的气体成分。他们利用下图提供的装置,自选试剂,提出了下列实验方案:按A→B→C→C→C→D→E顺序从左至右连接装置,检验乙二酸晶体受热分解生成的气体成分。
请你按整套装置从左至右的顺序填写下表中的空格:
| 仪器符号 | 仪器中所加物质 | 装置作用 |
| B | | |
| C | | |
| C | 氢氧化钠浓溶液 | |
| C | | |
| D | | |
| E | | |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)是一种重要的掺杂剂。实验室要用黄磷(白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如下图所示:(部分夹持装置略去)
已知黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。PCl3遇水会强烈水解生成H3PO3和HCl,遇O2会生成POCl3,POCl3溶于PCl3。PCl3、POCl3的熔沸点见下表:
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。某同学设计了如下实验方案并验证产物、探究反应原理。
(1)提出假设
实验Ⅰ:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能为________________。
猜测2:白色不溶物可能为MgCO3。
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3·yMg(OH)2]。
(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | ①气体成分为________ |
| 实验Ⅲ | ②取实验Ⅰ中的白色不溶物,洗涤,加入足量________ | ③________________ __________________ __________________ | 白色不溶物可能含有MgCO3 |
| 实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 产生白色沉淀 | ④溶液中存在________ |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
海带成分中碘的检验实验方案设计。
(1)干海带灼烧后,将海带灰放至小烧杯中加入适量蒸馏水,搅拌、煮沸冷却、过滤。将滤液分成四份放入四支试管中,并标为1、2、3、4号。
(2)在1号试管中滴入6滴稀硫酸后,再加入约3 mL H2O2溶液,滴入1%淀粉液1~2滴,观察到溶液立刻由褐色变成蓝色,离子方程式为 。
(3)在2号试管中加入2 mL新制的饱和氯水,振荡溶液,观察现象,离子反应方程式为 。2 min后把加入氯水的溶液分成两份。其中甲中再滴入1%淀粉液1~2滴,观察现象为 ,乙溶液中加入2 mL CCl4,振荡萃取,静置2 min后观察现象为 。
(4)在3号试管中加入食用碘盐3 g,振荡使之充分溶解后滴入6滴稀硫酸。在滴入1%淀粉液1~2滴,观察到溶液立刻由无色变成蓝色,相关的离子方程式为 。
(5)在4号试管中加入硝酸银溶液,振荡,再加入稀硝酸溶液。原想利用反应生成黄色沉淀来检验碘离子。通过实验发现生成白色沉淀。用此方法检验碘元素失败。导致此步失败的可能原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
硝基苯是重要的精细化工原料,是医药和染料的中间体,还可做有机溶剂。制备硝基苯的过程如下:①配制混酸:组装如下图反应装置。
取100 mL烧杯,用20 mL浓硫酸与浓硝酸18 mL配制混和酸,加入漏斗中。把18 mL苯加入三颈烧瓶中。
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀。
③在50-60℃下发生反应,直至反应结束。
④除去混和酸后,粗产品依次用蒸馏水和10%Na2CO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品。
已知(1)

(2)可能用到的有关数据列表如下
| 物质 | 熔点/℃ | 沸点/℃ | 密度(20 ℃) / g·cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 1,3-二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 |  | 83 | 1.4 | 易溶于水 |
| 浓硫酸 |  | 338 | 1.84 | 易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
固体硝酸盐加热易分解且产物较复杂。某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想:
甲:Mg(NO3)2、NO2、O2 乙:MgO、NO2、O2 丙:Mg3N2、O2 丁:MgO、NO2、N2
(1)实验前,小组成员经讨论认定猜想丁不成立,理由是____ ________。
查阅资料得知:2NO2+2NaOH=NaNO3+NaNO2+H2O
针对甲、乙、丙猜想,设计如下图所示的实验装置(图中加热、夹持仪器等均省略):
(2)实验过程
①取器连接后,放人固体试剂之前,关闭k,微热硬质玻璃管(A),观察到E 中有气泡连续放出,表明_ _______
② 称取Mg(NO3)2固体3 . 79 g置于A中,加热前通人N2以驱尽装置内的空气,其目的是________;关闭K,用酒精灯加热时,正确操作是先________然后固定在管中固体部位下加热。
③ 观察到A 中有红棕色气体出现,C、D 中未见明显变化。
④ 待样品完全分解,A 装置冷却至室温、称量,测得剩余固体的质量为1.0g
⑤ 取少量剩余固体于试管中,加人适量水,未见明显现象。
(3)实验结果分析讨论
① 根据实验现象和剩余固体的质量经分析可初步确认猜想_______是正确的。
② 根据D 中无明显现象,一位同学认为不能确认分解产物中有O2,因为若有O2,D中将发生氧化还原反应:_________________ ____(填写化学方程式),溶液颜色会退去;小组讨论认定分解产物中有O2存在,未检侧到的原因是_____________________。
③ 小组讨论后达成的共识是上述实验设计仍不完善,需改进装里进一步研究。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验室用浓硫酸和乙醇制取乙烯时,常会看到烧瓶中液体变黑,并在制得的乙烯中混
有CO2、SO2等杂质。某课外小组设计了如图所示装置,证明乙烯中混有CO2、SO2并验
证乙烯的性质。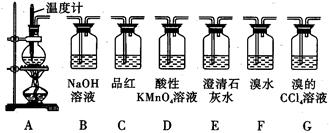
回答下列问题:
(1)烧瓶中素烧瓷片的作用是 。
(2)若要检验A中所得气体含有SO2,可将混合气体直接通入 (填图中代号,下同)装置;若要检验A中所得气体含有CH2=CH2,可将混合气体先通过B装置再通入 装置,也可将混合气体干燥后直接通入 装置。
(3)小明将从A出来的混合气体依次通过B、E、D、E,发现D前面的石灰水中无明显变化、D后面的石灰水变浑浊。请对出现该现象的原因进行合理猜想 。
(4)若要一次性将三种气体全部检验出来:
①检验的顺序是(填气体名称) ;
②上述装置组装的顺序中最简便的是:A→ ,证明C02存在的现象是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com