
| m |
| M |
| V |
| Vm |
| N |
| NA |
| 5.6L |
| 22.4L/mol |
| 6g |
| 30g/mol |
| 8g |
| 16g/mol |


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
| A、5、2、2 |
| B、7、3、2 |
| C、6、2、4 |
| D、5、3、4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
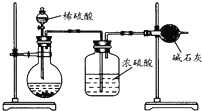 为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:
为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在自然界中存在的单质,一定具备化学性质稳定、不与其它物质发生反应这一特征 |
| B、100多年前,英国曾耗巨资改建高炉,试图延长CO和Fe2O3的接触时间,以减少CO的排放,这违背了化学反应都有一定限度这一基本原理 |
| C、在溶液中,有色物质参与的反应,可以用分光光度计来测定其化学反应速率 |
| D、虽然碳酸钙分解需要吸收大量的热,但在高温条件下也能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向NaClO溶液中通入少量二氧化硫 3ClO-+SO2+H2O═2HClO+SO42-+Cl- |
| B、碳酸氢钙与过量的NaOH溶液反应Ca2++HCO3-+OH-═CaCO3↓+H2O |
| C、用二氧化硫水溶液吸收溴蒸气:SO2+Br2+2H2O═SO42-+2H++2HBr |
| D、在碳酸氢铵稀溶液中加入足量的氢氧化钠稀溶液:NH4++OH-═NH3?H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com