
【题目】在气体参与的反应中,能使反应物中活化分子数和活化分子百分数同时增大的方法是( )
①增大反应物的浓度②升高温度③增大压强④加入催化剂
A. ①②B. ②③C. ②④D. ③④
科目:高中化学 来源: 题型:
【题目】锌钡白是一种白色颜料,工业上由ZnSO4与BaS溶液混合而成,BaS+ZnSO4=ZnS↓+BaSO4↓。请根据以下工业生产流程回答有关问题。
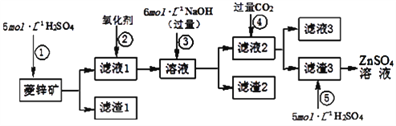
Ⅰ.ZnSO4溶液的制备与提纯:
有关资料:
a.菱锌矿的主要成分是ZnCO3,含少量SiO2、FeCO3、Cu2(OH)2CO3等;
b.Zn(OH)2与Al(OH)3相似,能溶于过量的NaOH溶液生成Na2ZnO2;
(1)为了达到综合利用、节能减排的目的,上述流程步骤④中的CO2可以来自于步骤____(选填①、②、③或⑤)。
(2)若步骤缺少②中加入的氧化剂为H2O2,写出反应的离子方程式_____________。
(3)滤渣2中主要成分为____________________(填化学式)。
(4)写出步骤④后产生滤渣3的反应的离子方程式________________。
(5)滤液3中含碳粒子的浓度大小顺序为_____________。
Ⅱ.BaS溶液的制备
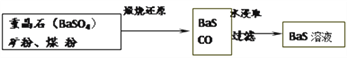
(6)写出“煅烧还原”反应的化学方程式_____________。BaSO4和BaCO3的Ksp数值接近,用平衡原理解释为什么BaCO3可溶于盐酸,而BaSO4难溶:______________。
Ⅲ.制取锌钡白
(7)如果上述工业生产流程中步骤⑤硫酸过量,则ZnSO4与BaS溶液混合制取锌银白产生的后果是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油产品含有多种含硫物质,如H2S、COS等。
(1)一种脱硫工艺为:真空K2CO3-克劳斯法。
①K2CO3溶液吸收H2S的反应为K2CO3+H2S=KHS+KHCO3,该反应的平衡常数的对数值为1gK=___。
(已知:H2CO3 lgK1=-6.4, lgK2=-10.3;H2S 1gK1=-7,lgK2=-19)
②已知下列热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H1 =-1172kJ·mol-1
2H2S(g)+O2(g)=2S(s)+2H2O(l) △H2 =-632kJ·mol-1
克劳斯法回收硫的反应为SO2气体和H2S气体反应生成S(s),则该反应的热化学方程式为___________________。同时,COS发生水解反应: COS(g)+H2O(g)![]() CO2(g)+H2S(g) △H>0,结合以上两个反应,克劳斯法选择反应温度为300℃,温度低有利于____,但温度过低会使硫析出,降低催化剂活性,反应过慢,以及不利于_______________。
CO2(g)+H2S(g) △H>0,结合以上两个反应,克劳斯法选择反应温度为300℃,温度低有利于____,但温度过低会使硫析出,降低催化剂活性,反应过慢,以及不利于_______________。
(2)石灰石料浆作为脱硫剂可有效吸收废气中的SO2,将CO2气体通入石灰石料浆罐对CaCO3脱硫剂进行活化处理可明显提高CaCO3脱硫的效率,活化后的主要脱硫反应之一为:2Ca2++2SO2+O2+3H2O = 2CaSO4·![]() H2O+4H+。
H2O+4H+。
①废气经脱硫后,除水蒸气外,________(填气体化学式)含量明显增多。
②其他条件一定,物料比为1.2时,脱硫反应的速率受Ca2+浓度的影响。图中a点是Ca(OH)2为脱硫剂时的脱硫效率,曲线表示CaCO3活化时间对脱硫效率的影响。

I.CaCO3与SO2反应的速率明显低于Ca(OH)2与SO2反应的速率,其原因是________。
II.a点和b点脱硫效率接近的原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ka(CH3COOH)=1.75×10-5, Ka (HCN)=6.2×10-10,下列说法正确的是
A. 0.1mol/L CH3COONa溶液与0.1mol/L KCN溶液:c(Na+)-c(CH3COO-)> c(K+)-c(CN-)
B. 20mL0.1 mol/L CH3COONa与10mL 0.1 mol/L HCl溶液混合后所得酸性溶液:c(Na+)>c(CH3COOH)>c(CH3COO-)
C. 0.2 mol/LHCN溶液与0.1 mol/L NaOH溶液等体积混合所得溶液:c(Na+)>c(CN-)>c(OH-)>c(H+)
D. 向浓度均为0.1mol/L的CH3COOH和HCN混合溶液中滴加0.1mol/LNaOH溶液,当恰好中和时所得溶液: c(CH3COOH)+c(HCN)+c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式,书写正确的是( )
A. 盐酸与石灰石反应CO32-+H+===CO2![]() +H2O
+H2O
B. 硫酸铜溶液中滴加氢氧化钡溶液Ba2++SO42-===BaSO4![]()
C. 氢氧化镁和盐酸反应:H++OH-===H2O
D. 氧化铁粉末溶于稀盐酸:Fe2O3+6H+===2Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,前者属于电解质,后者属于非电解质的是( )
A.NaCl晶体、BaSO4
B.铝、二氧化硫
C.液态的醋酸、酒精
D.熔融的KNO3、硫酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于分散系的说法,正确的是( )
A.根据体系的稳定性,可将分散系分为溶液、胶体和浊液
B.一种分散系的分散质可以是固态、液态或气态,但只能是纯净物
C.利用丁达尔效应可以区分溶液和胶体,它利用了光的衍射原理
D.火力发电厂的烟气管道里安装的静电除尘装置,它利用了胶体的电泳原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】117号元素以Uus表示。下列关于Uus元素的说法错误的是( )
A. 原子的价电子排布式是7s27p5B. 最高化合价是+7价
C. 其单质是双原子分子,常温常压下呈气态D. 阴离子具有很强的还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.1 mol H2O的质量为18g/mol
B.3.01×1023个SO3分子的质量为40g
C.CH4的摩尔质量为16g
D.标准状况下,1mol任何物质体积均为22.4L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com