
| A�� | �٢ڢ� | B�� | �ڢ� | C�� | �٢ۢܢ� | D�� | �ܢ� |
���� �ٷ�����˫ԭ�ӷ��ӣ�����ǵ�ԭ�ӷ��ӣ�
�ڵ�������������˫ԭ�ӷ��ӣ�
�۱�״���£�H2O��Һ�壻
�ܸ���n=$\frac{m}{M}$��N=nNA�������жϣ�
��һ��OH-�����к���10�����ӣ����N=nNA�����жϣ�
��� �⣺��ͬ�¡�ͬѹ�£���ͬ����ķ�������������ʵ�����ȣ���������˫ԭ�ӷ��ӣ�����ǵ�ԭ�ӷ��ӣ�����������ԭ�������ȣ��ʴ���
�ڱ�״���£�11.2L�����������ϵĵ��������������ʵ�����0.5mol����������������˫ԭ�ӷ��ӣ����Ա�״���£�11.2L�����������ϵĵ���������������ԭ����ΪNA������ȷ��
�۱�״���£�H2O��Һ�壬����Ħ������������ڸ����ʣ��ʴ���
��4��ʱˮ���ܶ�Ϊ1g/mL����5.4mLˮ������Ϊ5.4g�������ʵ���Ϊn=$\frac{5.4g}{18g/mol}$=0.3mol���ʺ�0.9molԭ�Ӽ�0.9NA��������ȷ��
��һ��OH-�����к���10�����ӣ�����0.1mol OH-��0.1��10NA=NA�����ӣ��ʴ���
��ѡB��
���� ���⿼�鰢���ӵ���������ؼ��㣬��Ŀ�ѶȲ���ע�����ʵ���ɡ��ṹ�������Լ����ʴ��ڵ���������;ۼ�״̬�����⣮


 �Ǽ�����������ϵ�д�
�Ǽ�����������ϵ�д� â���̸������Ծ�ϵ�д�
â���̸������Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ƽ��ʱSO2��ת���ʣ�A��B | |
| B�� | ���淴Ӧ�ӿ�ʼ��ƽ��ų���������A��B | |
| C�� | ƽ��ʱ�������������ʵ�����A��B | |
| D�� | ƽ��ʱ�Ļ�ѧ��Ӧ���ʣ�A��B |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ������̼ԭ�ӿ�����ͬһƽ���� ������̼ԭ�ӿ�����ͬһƽ���� | |
| B�� | 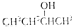 ������Ϊ2-��-1-���� ������Ϊ2-��-1-���� | |
| C�� | ��ϩ��������ϩ�ͱ������о�����̼̼˫�� | |
| D�� | C4H8����ϩ����ͬ���칹�干��4�֣���˳���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ϵͳ������2-�һ����� ϵͳ������2-�һ����� | |
| B�� | �ɷ���ʽΪC2H6O��ɵ�����һ���Ǵ����� | |
| C�� | ��������춡�黥Ϊͬϵ�� | |
| D�� | ��Ϊͬϵ������ʣ�����ɺͽṹ�����ƣ����Ի�ѧ����Ҳ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X3Y2 | B�� | X2Y | C�� | XY2 | D�� | XY3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������������Ե�Ҫ�������������������Լ�ƿ�� | |
| B�� | Һ��Ӧ������ĥ�ڲ������Լ�ƿ�У���������ˮ����ˮ�� | |
| C�� | ��ʹʪ��ĵ��۵⻯����ֽ����������һ�������� | |
| D�� | �������ھƾ��������þƾ��ӵ�ˮ����ȡ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ���������з����˷ܼ�����ʧ��ƽ��Ҳ�ܻ����������£�ij���˷ܼ��Ľṹ��ʽ��ͼ��ʾ���йظ����ʵ�˵������ȷ���ǣ�������
���������з����˷ܼ�����ʧ��ƽ��Ҳ�ܻ����������£�ij���˷ܼ��Ľṹ��ʽ��ͼ��ʾ���йظ����ʵ�˵������ȷ���ǣ�������| A�� | �����ʵķ���ʽΪC16H14O3 | |
| B�� | ��������KMnO4��Һ����ɫ��ȥ����֤����ṹ�д���̼̼˫�� | |
| C�� | 1mol�����ʷֱ���Ũ��ˮ��H2��Ӧʱ�������Br2��H2�ֱ�Ϊ4mol��7mol | |
| D�� | �÷����е�����̼ԭ�Ӳ����ܹ�ƽ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com