
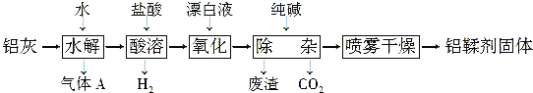
【题目】铝鞣剂[主要成分为Al(OH)2Cl]主要用于鞣制皮革。利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂的一种工艺如图:
回答下列问题:
(1)气体A能使湿润的红色石蕊试纸变蓝。铝灰在90 ℃水解生成A的化学方程式为____________。“水解”采用90℃而不在室温下进行的原因是_________________ 。
(2)“酸溶”时,Al2O3发生反应的离子方程式为____________________。
(3)“氧化”时,发生反应的离子方程式为________________________。
(4)“除杂”时产生废渣的主要成分为____(填化学式),对其合理的处理方法是回收后制成___。
(5)准确称取所制备的铝鞣剂mg,将其置于足量硝酸中,待样品完全溶解后,加入足量AgNO3溶液,充分反应,过滤、洗涤、干燥得固体ng.则样品中Al(OH)2Cl的质量分数为____(用含m、n的代数式表示)。
【答案】 AlN +3 H2O= NH3 ↑+Al(OH)3 加快AlN水解反应速率,降低NH3在水中的溶解度,促使NH3逸出 Al2O3+6H+=2Al3++3H20 2Fe2++2H++ClO﹣═2Fe3++Cl﹣+H2O Fe(OH)3 铁红 193n/287m×100%
【解析】铝灰主要成分为Al、Al2O3、AlN、FeO等,加水发生反应,AlN发生水解生成氢氧化铝和氨气,加入盐酸酸溶后,生成氯化铝溶液和氯化亚铁溶液,加入漂白剂氧化亚铁离子为铁离子,加入纯碱调节溶液pH使铁离子转化为氢氧化铁沉淀,采用喷雾干燥制备铝鞣剂。(1)AlN水解得到气体A是氨气,加热可以促进氮化铝水解生成氨气,有利于氨气的逸出;(2)酸溶时使用的酸是盐酸;(3)加入漂白液的作用是利用次氯酸根离子在酸溶液中的强氧化性,将氧化亚铁离子为铁离子;(4)由上述分析可知滤渣为氢氧化铁沉淀;可以回收利用生成铁红;(5)最终得到ng沉淀为AgCl的质量,根据氯离子守恒计算Al(OH)2Cl的质量,进而计算样品中Al(OH)2Cl的质量分数。
铝灰主要成分为Al、Al2O3、AlN、FeO等,加水发生反应,AlN发生水解生成氢氧化铝和氨气,加入盐酸酸溶后,生成氯化铝溶液和氯化亚铁溶液,加入漂白剂氧化亚铁离子为铁离子,加入纯碱调节溶液pH使铁离子转化为氢氧化铁沉淀,采用喷雾干燥制备铝鞣剂.
(1)AlN水解得到气体A是NH3,加热可以加快AlN水解反应速率,降低NH3在水中的溶解度,促使NH3逸出;(2)由流程图可知,酸溶时使用的酸是盐酸;(3)加入漂白液的作用是利用次氯酸根离子在酸溶液中的强氧化性,将氧化亚铁离子为铁离子,反应离子方程式为:2Fe2++2H++ClO-═2Fe3++Cl-+H2O;(4)由上述分析可知,滤渣为Fe(OH)3沉淀;可以回收利用生成铁红;(5)最终得到ng沉淀为AgCl的质量,根据氯离子守恒,Al(OH)2Cl的质量=![]() ×96.5g/mol,故样品中Al(OH)2Cl的质量分数为(
×96.5g/mol,故样品中Al(OH)2Cl的质量分数为(![]() ×96.5g/mol÷mg)×100%=
×96.5g/mol÷mg)×100%=![]() ×100%。
×100%。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列关于淀粉和纤维素的叙述中,不正确的是( )
A.它们都是混合物
B.它们互为同分异构体
C.它们都能水解生成葡萄糖
D.它们都是天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是
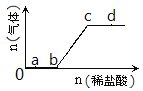
A. a点对应的溶液中:Na+、OH-、SO42-、NO3-
B. b点对应的溶液中:K+、Al3+、MnO4-、Cl-
C. c点对应的溶液中:Na+、Ca2+、NO3-、Cl-
D. d点对应的溶液中:K+、Fe2+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气在工农业生产中有重要应用。
(1)氮气用于工业合成氨,写出氮气的电子式 __________;
(2)如下图所示,向NaOH固体上滴少量浓氯化铵溶液,迅速盖上盖,观察现象。

①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为_________。
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是_____(写化学式,一种即可)。
③FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2++2NH3·H2O===Fe(OH)2↓+2NH![]() 和____________。
和____________。
(3)空气吹脱法是目前消除NH3对水体污染的重要方法。在一定条件下,向水体中加入适量NaOH可使NH3的脱除率增大,解释其原因____。
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为______,若反应中有0.3 mol电子发生转移时,生成亚硝酸的质量为______ g(小数点后保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关热化学方程式书写与对应表述均正确的是
A. 稀硫酸与0.1 mol·L-1 NaOH溶液反应:H+(aq)+OH-(aq)=H2O(l) ΔH=+57.3 kJ·mol-1
B. 在101 kPa下H2(g)的燃烧热为285.8 kJ·mol-1,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g) ΔH=+285.8 kJ·mol-1
C. 已知CH3OH的燃烧热为726.8 kJ·mol-1,则有CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(g) ΔH=-726.8 kJ·mol-1
O2(g)=CO2(g)+2H2O(g) ΔH=-726.8 kJ·mol-1
D. 已知9.6 g硫粉与11.2 g铁粉混合加热生成17.6 g FeS时放出19.12 kJ热量,则Fe(s)+S(s)=FeS(s) ΔH=-95.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)L的元素符号为________ ;M在元素周期表中的位置为________________;五种元素的原子半径从大到小的顺序是_________________(用元素符号表示)。
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B ,A的沸点比同主族其他气态氢化物___________(填“高”或“低”),原因是________________________________,B中存在的化学键类型为____________。
A极性共价键 B非极性共价键 C 离子键
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为__________,其最高价氧化物对应的水化物化学式为__________。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。
a +99.7 kJ·mol-1 b +29.7 kJ·mol-1 c -20.6 kJ·mol-1 d -241.8 kJ·mol-1

(4)Y、硅与硫三种元素非金属性由强到弱的顺序为________________(用元素符号表示)。某同学用如图所示装置验证Y、硅与硫三种元素非金属性强弱(夹持仪器已略去,气密性已检验)。Ⅰ、Ⅱ、Ⅲ所加入的试剂分别为:_________________________(用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O是一种鲜红色粉末状固体,几乎不溶于水,在酸性溶液中歧化为二价铜和铜单质。可用于制造船底防污漆等。某校合作学习小组的同学设计实验验证其某些性质及其胶体的制法。回答下列问题:
(1)甲组同学检验H2还原CuO所得的红色粉末中是否有Cu2O。取反应产物少许加入试管中,加入足量的试剂X并搅拌,若发现溶液变蓝且仍有剩余固体,则试剂X可选用_________(填序号)。
a.FeCl3溶液 b.硝酸 c.稀硫酸 d. H2O2酸性溶液
(2)乙组同学在两支试管中分别加入少量Cu2O,一支中加入稀硝酸,固体溶解同时产生NO气体,Cu2O表现_______________性;另一支加入硫酸酸化的KMnO4溶液,溶液紫色褪去得蓝色溶液,反应的离子方程式为______________。
(3)丙组同学取少量Cu2O与黑色的Cu2S混合加强热,产生大量的气体同时得到红色固体粉末,该反应的化学方程式为____________________。
(4)丁组同学向0.1mol·L-1 的(CH3COO)2Cu溶液中加入0.02mol·L-1的N2H4的水溶液,控制pH=7~8,得到红色透明液体,能说明该分散系属于胶体的简单方法是____________。已知制备过程中有N2放出,制备反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. Na2O2中阴阳离子个数比为1:2
B. 金属钠着火,可用泡沫灭火器扑灭
C. 非金属氧化物都是酸性氧化物
D. 当钠与硫酸铜溶液反应时,可观察到大量的红色固体物质生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com