
【题目】下列有关化学反应速率和限度的说法中,不正确的是
A. 实验室用H2O2分解制O2,加入MnO2后,反应速率明显加快
B. 在金属钠与足量水反应中,增加水的量能加快反应速率
C. 2SO2+O2![]() 2SO3反应中,SO2不能全部转化达为SO3
2SO3反应中,SO2不能全部转化达为SO3
D. 实验室用碳酸钙和盐酸反应制取CO2,若将块状碳酸钙粉碎,会加快反应
科目:高中化学 来源: 题型:
【题目】Ⅰ.工业合成氨与制备硝酸一般可连续生产,回答下列问题:
(1)工业生产时,制取氢气的一个反应为:CO+H2O(g)![]() CO2+H2。T℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=_______(填计算结果)。
CO2+H2。T℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=_______(填计算结果)。
(2)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为: 。
(3)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极在碱性条件下发生反应的电极反应式为 。
Ⅱ.甲醇是一种重要的有机化工原料,可用于制取甲醚。一定温度下,在三个体积为1.0L的恒容密闭容器中发生反应:2CH3OH(g)![]() CH3OCH3(g)+ H2O(g)。
CH3OCH3(g)+ H2O(g)。
容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
II | 387 | 0.40 | a | b |
III | 207 | 0.20 | 0.090 | 0.090 |
(4) 容器I中的反应达到平衡时所需的时间_______(填“大于”“小于”或等于)容器II中的。
(5) a=
(6) 下列说法中能说明该反应达到平衡状态的是 。(填字母)
A.容器中压强不变
B.混合气体中c(CH3OCH3) 不变
C.混合气体的密度不变
D.单位时间内生成1 mol CH3OCH3 同时消耗2molCH3OH
(7)已知下面两个反应(m、n均大于0):
反应①:CO(g)+2H2(g) ![]() CH3OH(g) ΔH=-m kJ·mol-1
CH3OH(g) ΔH=-m kJ·mol-1
反应②:2CO(g)+4H2(g) ![]() CH3OCH3(g)+H2O(g) ΔH= -n kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH= -n kJ·mol-1
则下列m与n的关系中,正确的是 (填字母)。
A.n﹥2m B.m﹥2 n C.2m﹥n D.m﹥3n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】O2F2可以发生反应:H2S+4O2F2=SF6+2HF+4O2,下列说法正确的是( )
A.氧气是氧化产物
B.O2F2既是氧化剂又是还原剂
C.若生成4.48LHF,则转移0.8mol电子
D.还原剂与氧化剂的物质的量之比为1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究足量锌与浓硫酸的反应,某研究小组进行如下实验。取足量锌与浓H2SO4充分反应,对于制得的气体,有同学认为可能混有杂质。
(1)研究小组所制得的气体中混有的主要杂质气体可能是:__________(填分子式)。产生这种结果的主要原因是: (用化学方程式和必要的文字加以说明)
(2)为证实相关分析,该化学小组的同学设计实验,组装了图1装置,对所制了的气体进行探究.

①装置C中加入的试剂是:__________;装置D中加入的试剂是:__________.
②装置F中加入的试剂是:__________;U型管G的作用为:______________.
③有同学认为A、B间应增加图中的甲装置,该装置的作用为:______________.
④证明反应生成SO2和H2的实验现象是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废液中含有Cu2+、Mg2+、Zn2+等离子,为将其回收利用,再采用了如下工艺
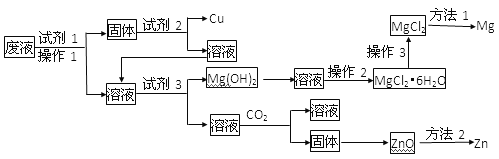
已知Zn(OH)2的性质与Al(OH)3相似
所用试剂在下列试剂中选择
① 铁粉 ②锌粉 ③稀HNO3 ④稀H2SO4 ⑤稀HCl ⑥稀氨水 ⑦NaOH溶液 ⑧石灰水
请回答下列问题:
(1)试剂1、试剂2、试剂3分别可以是________、________、________(填编号)
(2)操作2是_______________、______________、______________
(3)操作3是________________________________
(4)加过量CO2时发生反应的离子方程式________________________
(5)用离子方程式解释试剂3能分离出Mg(OH)2的原理:__________________、_________________
(6)在金属冶炼方法中方法1是_________方法2是____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的五种盐X、Y、Z、M、N,它们的阴离子可能是SO![]() 、Cl-、NO
、Cl-、NO![]() 、CO
、CO![]() ,阳离子可能是Ag+、NH
,阳离子可能是Ag+、NH![]() 、Na+、Al3+、Cu2+、Ba2+、Fe3+,已知:
、Na+、Al3+、Cu2+、Ba2+、Fe3+,已知:
①M的焰色反应呈黄色。
②五种盐均溶于水,水溶液均为无色。
③X的溶液呈中性,Y、Z、N的溶液呈酸性,M的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有X、Z的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,N和Z的溶液中生成沉淀,继续加氨水,Z中沉淀消失。
⑥把X的溶液分别加入到Y、Z、N的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,所含阴离子相同的两种盐的化学式是__________________
(2)M溶液显碱性的原因是(用离子方程式表示)______________________
(3)X和Z的溶液反应的离子方程式是_______________________
(4)N和氨水反应的离子方程式是___________________________
(5)若要检验Y中所含的阳离子,正确的实验方法是____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于烷烃的叙述不正确的是( )
A.分子式符合CnH2n+2的烃一定是烷烃
B.烷烃均能与氯水发生取代反应
C.正戊烷的熔沸点比乙烷的高
D.烷烃不能被酸性高锰酸钾等强氧化剂氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列叙述正确的是( )
A.煤的干馏和煤的液化均是物理变化
B.海水淡化的方法有蒸馏法、电渗析法等
C.棉、丝、毛、油脂都是天然有机高分子化合物
D.石油裂化的目的是得到乙烯、丙烯等化工原料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com