
| A. | 通入CO2气体产生蓝色沉淀 | |
| B. | 该溶液中Na+、NH4+、NO3-、Mg2+可以大量共存 | |
| C. | 与H2S反应的离子方程式:Cu2++S2-=CuS↓ | |
| D. | 与过量浓氨水反应的离子方程式:Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+ |
分析 A.硫酸铜溶液与二氧化碳不反应;
B.该组离子之间不反应;
C.H2S在离子反应中保留化学式;
D.与过量浓氨水反应,生成络离子.
解答 解:A.硫酸铜溶液与二氧化碳不反应,不能生成沉淀,故A错误;
B.该组离子之间不反应,可大量共存,故B正确;
C.H2S在离子反应中保留化学式,则离子方程式为Cu2++H2S=CuS↓+2H+,故C错误;
D.与过量浓氨水反应,生成络离子,则与过量浓氨水反应的离子方程式为Cu2++4NH3•H2O=[Cu(NH3)4]2++4H2O,故D错误;
故选B.
点评 本题考查离子共存及离子反应,为高频考点,把握离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、络合反应的判断,题目难度不大.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,2.24L HF中所含有的分子数约为6.02×1022 | |
| B. | 3.2克的Cu与足量的浓硝酸反应生成的气体分子数约为6.02×1022 | |
| C. | 含有6.02×1023个中子的D2O的质量为2.0g | |
| D. | pH=2的硫酸氢钠溶液中的硫酸根离子数约为6.02×1021 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 35.9g | B. | 30.8g | C. | 28.1g | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物(如图所示),发生如下反应:3X(g)+Y(g)?2Z(g)△H<0.保持温度不变,测得平衡时的有关数据如表:下列说法正确的是( )
在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物(如图所示),发生如下反应:3X(g)+Y(g)?2Z(g)△H<0.保持温度不变,测得平衡时的有关数据如表:下列说法正确的是( ) | 恒容容器甲 | 恒压容器乙 | |
| X的物质的量(mol) | n1 | n2 |
| Z的体积分数 | φ1 | φ2 |
| A. | 平衡时容器乙的容积一定比反应前小 | |
| B. | 平衡时容器甲的压强一定比反应前小 | |
| C. | n2>n1 | |
| D. | φ2<φ1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,0.56 L丙烷中含有共价键的数目为0.2NA | |
| B. | 常温常压下,6.4 g氧气和臭氧中含有的分子总数为0.2NA | |
| C. | 一定条件下,5.6 g铁与浓硫酸恰好反应,转移的电子数目一定为0.2NA | |
| D. | 常温下,20 L pH=12的Na2CO3溶液中含有的OH-离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | F的原子结构示意图: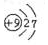 | |
| B. | CH3CH2COOH:从分类角度看该物质属于羧酸 | |
| C. | 次氯酸的电子式: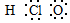 | |
| D. | 壬烷和癸烷,丁烷和新戊烷均为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
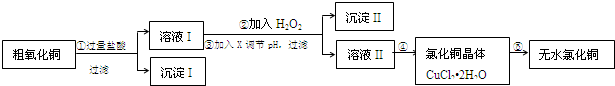
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| Fe2+ | 7.0 | 9.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com