
对于常温下pH为1的硝酸溶液,下列叙述正确的是( )
A.该溶液1 mL稀释至100 mL后,pH等于3
B.向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和
C.该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为10-12
D.该溶液中水电离出的c(H+)是pH为3的硝酸中水电离出的c(H+)的100倍
科目:高中化学 来源:2016-2017学年海南省高二上期中文化学卷(解析版) 题型:选择题
随着人们生活节奏的加快,方便的小包装食品己进入千家万户。为延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中应放入的化学物质是( )
A.无水硫酸铜、蔗糖 B.硅胶、硫酸亚铁
C.无水硫酸铜、硫酸亚铁 D.生石灰、食盐
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西柳州铁路一中高二上段考文化学卷(解析版) 题型:选择题
反应2SO2+O2 2SO3在密闭容器中进行。下列关于该反应的说法错误的是
2SO3在密闭容器中进行。下列关于该反应的说法错误的是
A.升高温度能加快反应速率  B.使用恰当的催化剂能加快反应速率
B.使用恰当的催化剂能加快反应速率
C.增大O2的浓度能加快反应速率 D.SO2与O2能100%转化为SO3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西柳州铁路一中高二上段考理化学卷(解析版) 题型:填空题
某二元酸(化学式用H2B表示)在水中的电离方程式:H2B=H++HB-,HB- H++B2-。回答下列问题:
H++B2-。回答下列问题:
(1) NaHB溶液显 (填“酸性”“中性”或“碱性”)。理由是 。
(2)在0.1 mol·L-1的Na2B溶液中,下列粒子浓度关系式正确的是 。
A.c(B2-)+c(HB-)+c(H2B)=0.1 mol·L-1
B.c(OH-)=c(H+)+c(HB-)
C.c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-)
D.c(Na+)=2c(B2-)+2c(HB-)
(3)0.1 mol·L-1 Na2B溶液中各种离子浓度由大到小的顺序是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西柳州铁路一中高二上段考理化学卷(解析版) 题型:选择题
某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是( )
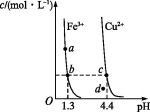
A.Ksp[Fe(OH)3]<Ksp[Cu(OH)2]
B.c、d两点代表的溶液中c(H+)与c(OH-)乘积相等
C.加适量NH4Cl固体可使溶液由a点变到b点
D.Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西柳州铁路一中高二上段考理化学卷(解析版) 题型:选择题
室温下,若溶液中由水电离产生的c(OH-)=1×10-14 mol·L-1, 满足此条件的溶液中一定可以大量共存的离子组是( )
满足此条件的溶液中一定可以大量共存的离子组是( )
A.Al3+、Na+、NH4+、Cl- B.K+、Na+、Cl-、AlO2-
C. K+、Na+、Cl-、NO3- D.K+、CO32-、SO42-、NO3-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高一上期中化学卷(解析版) 题型:选择题
下列叙述正确的是
A.液态HC1不能导电,所以HC1是非电解质
B.酸性氧化物一定是非金属氧化物
C.在水溶液中能电离产生H的化合物不定是酸
D.盐、碱一定含有金属元素
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上综合测试三化学卷(解析版) 题型:填空题
某经济开发区将钛冶炼厂与氯碱厂、甲醇厂组成了一个产业链(如图所示),大大地提高了资源利用率,减少了环境污染。
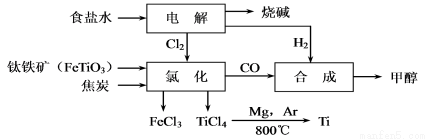
请填写 下列空白:
下列空白:
(1)电解饱和食盐水的离子方程式 。若用石墨作电极电解500 mL饱和食盐水,当两极共收集到标准状况下的气体1.12 L(不考虑气体的溶解)时,所得溶液的pH为 (假设反应前后溶液体积不变)。
(2)写出钛铁矿经氯化得到四氯化钛的化学方程式: 。
(3)由CO和H2合成甲醇的方程式是:CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
①已知该反应在300℃时的化学平衡常数为0.27,该温度下将2 mol CO、3 mol H2和2 mol CH3OH充入容积为2 L的密闭容器中,此时反应将 (填字母编号)
A.向正反应方向进行 B.向逆反应方向进行 C.处于平衡状态
②若不考虑生产过程中物质的任何损失,该产业链中每合成19.2 t甲醇,至少需额外补充H2 t。
(4)用甲醇-空气碱性(KOH)燃料电池作电源电解精炼粗铜(含铁、锌等杂质,如图),在接通电路一段时间后纯Cu质量增加6.4 g。
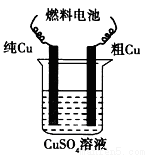
请写出电解精炼过程中杂质参加的一个电极反应: 。
②燃料电池正极消耗氧气的体积是 (标准状况)。
(5)氢气是合成氨气的重要原料。
已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H= -908 kJ·mol-l
N2(g)+O2(g)=2NO(g) △H=+180kJ·mol-l
写出氨气被一氧化氮氧化生成氮气和气态水的热化学方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com