

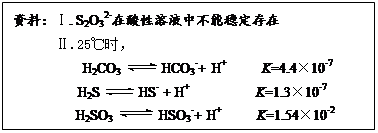
 NH3 + HClO(不写可逆号扣1分)
NH3 + HClO(不写可逆号扣1分) Fe2+,不会得到氯气,所以铁电极作阴极,石墨电极上的电极反应式为2Cl- - 2e- = Cl2↑。
Fe2+,不会得到氯气,所以铁电极作阴极,石墨电极上的电极反应式为2Cl- - 2e- = Cl2↑。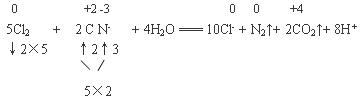
 NH3 + HClO,HClO具有强氧化性,能消毒杀菌。
NH3 + HClO,HClO具有强氧化性,能消毒杀菌。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源:不详 题型:单选题
| A.稀硝酸和过量铁屑反应:Fe+4H++NO3-=Fe3++NO↑+2H2O |
| B.向硫酸氢铵溶液中加入少量氢氧化钠溶液:NH4++OH-=NH3↑+H2O |
| C.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| D.H2C2O4使酸性KMnO4溶液褪色:5H2C2O4+6H++2MnO4-=10CO2↑+2Mn2++8H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜跟稀硝酸反应:3Cu+ 8H++2NO3-=3Cu2++2NO↑+4H2O |
| B.实验室用大理石和稀盐酸制取CO2:2H+ + CO32-=CO2↑+ H2O |
| C.金属铁与稀硫酸反应:2Fe+6H+=2Fe3+ + 3H2↑ |
| D.钠与水反应: Na+H2O=Na++OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氨水与亚硫酸溶液混合:NH3·H2O+H+=NH4++H2O |
| B.SO2通入漂白粉溶液中:Ca(ClO)2+SO2+H2O=CaSO3↓+2HClO |
C.铜与浓硫酸共热:Cu+4H++SO42- Cu2++SO2↑+2H2O Cu2++SO2↑+2H2O |
| D.把H2S通入CuSO4溶液中:H2S+Cu2+=CuS↓+2H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用浓盐酸检验氨:NH3+HCl=NH4Cl |
B.碳酸钠溶液显碱性:CO32—+H2O HCO3—+OH- HCO3—+OH- |
| C.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+ |
| D.长期盛放石灰水的试剂瓶内壁出现白色固体:Ca(OH)2+CO2=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.5mol/L氢氧化钙溶液和0.5mol/L碳酸氢镁溶液等体积混合反应:Ca2++ OH-+ HCO3=CaCO3↓+H2O |
| B.少量的SO2通入Ca(ClO)2溶液中反应的离子方程式为:SO2+H2O+Ca2++2ClO- = CaSO3↓+2HClO |
| C.将11.2L标准状况下的氯气通入200mL2mol/L的FeBr2溶液中,离子反应方程式为:2Fe2++8Br-+5Cl2=2Fe3++4Br2+10Cl- |
| D.某锂电池电极总反应为:4Li+2SOCl2 = 4LiCl+S+SO2↑,则正极反应为:2SOCl2 + 4e-= 4Cl-+S +SO2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯气溶于水:Cl2+H2O=2H++Cl-+ClO- |
| B.硫酸铝溶液中加入足量氨水:Al3++4OH-=[Al(OH)4]- |
| C.FeSO4溶液与稀硝酸反应:3Fe2++NO3—+4H+=3Fe3++NO↑+2H2O |
| D.碳酸氢铵和足量氢氧化钠溶液反应:NH4++OH-=NH3·H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钠与硫酸铜溶液反应:Cu2++2Na=2Na++Cu |
| B.铁屑溶于过量稀硝酸:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O |
| C.石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O |
| D.FeI2溶液中通人少量氯气:2Fe2++Cl2=2Fe3++2Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com