
【题目】钯的化合物氯化钯可用来检测有毒气体CO,发生反应的化学方程式为:![]() 。下列说法正确的是()
。下列说法正确的是()
A.题述反应条件下还原性:CO>Pd
B.题述反应中PdCl2被氧化
C.生成22.4 L CO2时,转移的电子为2 mo1
D.CO气体只有在高温下才能表现还原性
科目:高中化学 来源: 题型:
【题目】科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是

A. WZ的水溶液呈碱性
B. 元素非金属性的顺序为X>Y>Z
C. Y的最高价氧化物的水化物是中强酸
D. 该新化合物中Y不满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种制备高效漂白剂NaC1O2的实验流程如图所示,反应I的化学方程式为: 3NaC1O3+4SO2+3H2O=2C1O2+Na2SO4+3H2SO4+NaCl,下列说法正确的是
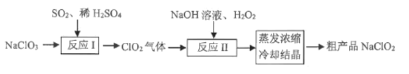
A.NaClO2的漂白原理与SO2相同
B.反应I中氧化产物和还原产物物质的量比为4:3
C.反应II中H2O2做氧化剂
D.实验室进行蒸发操作通常在坩埚中进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碲(Te)具有两性特征,铜阳极泥是提取碲的主要原料,碲在铜阳极泥中主要以MezTeCMe表 示金属Cu、Pb、Au、Ag等)的形式存在。
(1)利用“氯化浸出-还原法”制备Te的工艺流程如下所示。
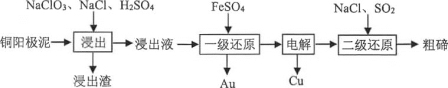
①浸出液的主要成分为CuSO4、HAuCu、H2TeO3,则浸出渣的主要成分 为____(填化学式);“浸出”过程中有少量污染性气体生成,该气体是_______(填物质名称)
②已知HAuCU是一种强酸,则“一级还原”过程中发生反应的离子方程式为_________。
③欲得到64g碲,则“二级还原”过程中至少需通入____mol SO2。 “氧化碱浸-电解法”指的是在氧化剂的作用下,Cu2Te与NaOH溶液反应生成Na2TeO3和Cu(OH)2,经电解即可获得Te。
①以空气为氧化剂进行“氧化碱浸”的化学方程式为______。
②电解过程中,阴极的电极反应式为______。
③与“氯化浸出-还原法”相比“氧化碱浸-电解法”的优点是____(任写一点)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,11.2L NO2完全溶于水,转移电子数为0.5NA
B.20g D2O和HTO两种水的组合中含有的中子数为10NA
C.一定温度下,lmol H2和足量碘蒸气反应产生的H-I键数目为2NA
D.标准状况下,22.4L的SO3中含有的O原子数目为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价——物质类别关系图如下。
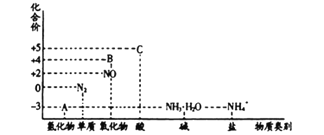
回答下列问题:
(1)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是:__________
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式: _______________;
(3)实验室中,检验溶液中含有NH4+的操作方法是: __________________________;
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式_____________,当反应消耗3.36L (标准状况) 物质B时,转移电子的物质的量为__________________________。
(5)将32g铜与140 mL一定浓度的C溶液反应,铜完全溶解产生的气体在标准状况下的体积为11.2L。
①参加反应的C的物质的量为__________________________;
②待产生的气体全部释放后,向溶液中加入VmLamol·L-1 的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原C溶液的浓度为________ mol·L-1
③欲使铜与C反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要通入O2_____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁镍蓄电池充放电时的总反应:![]() ,下列有关该电池的说法不正确的是( )
,下列有关该电池的说法不正确的是( )
A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe
B.电池放电时,负极反应为![]()
C.电池充电过程中,阴极附近溶液的pH降低
D.电池充电时,阳极反应为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】漂白粉主要成分可用下式表示:
Ca(OH)2·3CaCl(ClO)·nH2O,用过量的盐酸和漂白粉作用可生成Cl2。Cl2与漂白粉的质量比叫做漂白粉的“有效氯”。现有一种漂白粉的“有效氯”为0.355,则式中的n值约为
A、7.5 B、8.0 C、9.5 D、11.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物结构和性质的说法错误的是
A. 分子式为C5H10O2且能与 NaHCO3反应放出气体的结构共有4种
B. 石油是混合物,可通过分馏得到汽油、煤油等纯净物
C. 苯甲酸(![]() )分子中所有原子可能位于同一平面
)分子中所有原子可能位于同一平面
D. 1mol盐酸美西律( )最多可与3 mol H2发生加成
)最多可与3 mol H2发生加成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com