
【题目】下列各物质中,互为同系物的是( )
A.HCOOCH3和 CH3COOH
B.CHCl3和氯乙烷
C.![]() 和
和 ![]()
D.![]() 和
和 ![]()
科目:高中化学 来源: 题型:
【题目】在0.2L NaCl、MgCl2的混合溶液中,部分离子浓度大小如图所示,回答下列问题: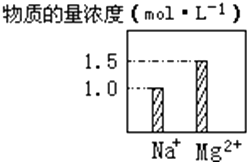
(1)该混合溶液中,Na+的物质的量为moL,MgCl2的物质的量为moL,Cl﹣的物质的量为moL.
(2)该混合溶液中含溶质的总质量为 g.
(3)将该混合溶液加水稀释至体积为 1L,稀释后溶液中Cl﹣的物质的量浓度为moLL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列给定条件的溶液中,一定能大量共存的离子组是( )
A.加水稀释 ![]() 增大的溶液:K+、Na+、SO42﹣、AlO2﹣
增大的溶液:K+、Na+、SO42﹣、AlO2﹣
B.常温下 ![]() =0.1 mol/L的溶液:K+、Na+、SiO32﹣、NO3﹣
=0.1 mol/L的溶液:K+、Na+、SiO32﹣、NO3﹣
C.铁片加入产生气泡的溶液:Na+、NH4+、I﹣、NO3﹣
D.NaHCO3溶液:K+、Na+、SO42﹣、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定的四种溶液中加入以下各种离子,能大量共存的是( )
A. pH<7的溶液:Cu2+ Na+ Mg2+ NO3-
B. 滴加酚酞溶液显红色的溶液:Fe3+ NH4+ Cl- NO3-
C. 所含溶质为NaOH的溶液:K+ SO42- NO3- H+
D. 在碱性溶液:K+ HCO3- Br- Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤化工中两个重要反应为: ①C(s)+H2O(g)═H2(g)+CO(g)△H=+131.3kJmol﹣1 ,
②CO(g)+H2O(g) ![]() CO2(g)+H2(g).
CO2(g)+H2(g).
(1)下列说法正确的是 .
A.当反应①的容器中混合气体的密度不再变化时反应达到最大限度
B.反应②的熵变△S>0
C.反应①中增加C固体的量能增大反应速率
D.在反应中②及时分离出产生的H2对正反应速率无影响
(2)若工业上要增加反应①的速率,最经济的措施为 .
(3)现将不同量的CO(g)和H2O(g)分别通入2L恒容密闭容器中进行反应,得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 | ||
CO | H2O | H2 | CO2 | |||
I | 650 | 4 | 2 | 1.6 | 1.6 | 5 |
Ⅱ | 900 | 2 | 1 | 0.5 | 0.5 | 3 |
Ⅲ | 900 | a | b | c | d | t |
①实验I中,从反应开始到反应达到平衡时,H2O的平均反应速率为 .
②CO(g)和H2O(g)反应的△H0 ( 填“大于”、“小于”或“等于”)
③实验III中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是 , 与实验Ⅱ相比,化学平衡常数(填“增大”、“减小”或“不变”).
④若在900℃时,实验II反应达到平衡后,向此容器中再加入1mol CO、0.5mol H2O、0.2mol CO2、0.5mol H2 , 平衡向方向移动(填“正反应”、“逆反应”“不移动”).
(4)CO、H2可用于甲醇和甲醚,其反应为(m、n均大于0): 反应①:CO(g)+2H2(g)CH3OH(g)△H=﹣mkJmol﹣1
反应②:2CO(g)+4H2(g)CH3OCH3(g)+H2O(g)△H=﹣nkJmol﹣1
反应③:2CH3OH(g)CH3OCH3(g)+H2O(g)△H<0
则m与n的关系为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】举世瞩目的中国探月工程三期再入返回试验器于2014年10月24日凌晨成功发射,为实现月球采样和首次地月往返踏出了成功的第一步.探月工程三期的主要目标是实现无人自动采样返回,突破月面采样、月面上升、月球轨道交会对接等核心关键技术.已知所用火箭推进剂为肼 (N2H4)和过氧化氢(H2O2),火箭箭体一般采用钛合金材料. 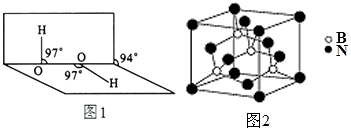
请回答下列问题:
(1)N2H4、H2O2分子中电负性最大的元素在周期表中的位置为 , 第一电离能最大的元素为 .
(2)钛的原子序数为22,其基态电子排布式示意图为 .
(3)1mol N2H4分子中含有的键数目为 .
(4)H2O2分子结构如图1,其中心原子杂化轨道为 , 估计它难溶于CS2 , 简要说明原因
(5)氮化硼其晶胞如图2所示,则处于晶胞顶点上的原子的配位数为 , 若立方氮化硼的密度为ρ gcm﹣3 , 阿伏加德罗常数为NA , 则两个最近N原子间的距离为cm.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤化工中两个重要反应为: ①C(s)+H2O(g)═H2(g)+CO(g)△H=+131.3kJmol﹣1 ,
②CO(g)+H2O(g) ![]() CO2(g)+H2(g).
CO2(g)+H2(g).
(1)下列说法正确的是 .
A.当反应①的容器中混合气体的密度不再变化时反应达到最大限度
B.反应②的熵变△S>0
C.反应①中增加C固体的量能增大反应速率
D.在反应中②及时分离出产生的H2对正反应速率无影响
(2)若工业上要增加反应①的速率,最经济的措施为 .
(3)现将不同量的CO(g)和H2O(g)分别通入2L恒容密闭容器中进行反应,得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 | ||
CO | H2O | H2 | CO2 | |||
I | 650 | 4 | 2 | 1.6 | 1.6 | 5 |
Ⅱ | 900 | 2 | 1 | 0.5 | 0.5 | 3 |
Ⅲ | 900 | a | b | c | d | t |
①实验I中,从反应开始到反应达到平衡时,H2O的平均反应速率为 .
②CO(g)和H2O(g)反应的△H0 ( 填“大于”、“小于”或“等于”)
③实验III中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是 , 与实验Ⅱ相比,化学平衡常数(填“增大”、“减小”或“不变”).
④若在900℃时,实验II反应达到平衡后,向此容器中再加入1mol CO、0.5mol H2O、0.2mol CO2、0.5mol H2 , 平衡向方向移动(填“正反应”、“逆反应”“不移动”).
(4)CO、H2可用于甲醇和甲醚,其反应为(m、n均大于0): 反应①:CO(g)+2H2(g)CH3OH(g)△H=﹣mkJmol﹣1
反应②:2CO(g)+4H2(g)CH3OCH3(g)+H2O(g)△H=﹣nkJmol﹣1
反应③:2CH3OH(g)CH3OCH3(g)+H2O(g)△H<0
则m与n的关系为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是一种形状酷似罗马两面神Janus的有机物结构简式,化学家建议将该分子叫做“Janusene”,有关Janusene的说法正确的是( ) 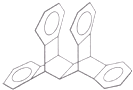
A.Janusene的分子式为C30H22
B.Janusene属于苯的同系物
C.Janusene苯环上的一氯代物有6种
D.Janusene既可发生氧化反应,有可发生还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com