

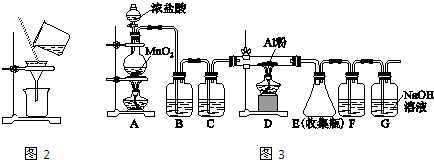
���� ��1��Ϊ�˷�ֹҺ�彦�����ڹ���ʱӦ�ý�©���ļ��첿�ֽ����ձ����ڱڣ�
��2�����������֪��������Ӧ�ø��������Ӻ�笠����ӣ����ж��Ƿ�ϴ��������ȡ�������һ��ϴ��Һ�����������ữ����������Һ�����жϣ������ɰ�ɫ��������˵��û��ϴ�Ӹɾ�����û�г������ɣ���˵���Ѿ�ϴ�Ӹɾ���
��3����ͼ3װ���Ʊ��Ȼ���ʱ������Ũ���������������A�з�Ӧ���������������Ȼ����ӷ��������Ƶõ����������Ȼ����ˮ������B�зű���NaCl��Һ����ȥ�����е��Ȼ��⣬C����Ũ���������ɵ��Ȼ�����ˮ�⣬��Ӧ��β��Ϊ������������������������������E��G֮���Fװ���з�Ũ�����ֹ����������Һ�е�ˮ����Eװ�ã�F��G������������������ˮ�������ü�ʯ�Ҵ��棬�ݴ˴��⣻
��4��Cl2��Ca��OH��2��Ӧ�����Ȼ��ƺʹ�����ƣ�
��5��Na2SO3��Һ����������������ԭ��Ӧ������������Ӻ������ӣ����ݵ���غ��Ԫ���غ���д���ӷ���ʽ��
��� �⣺��1������ʱӦ�ý�©���ļ��첿�ֽ����ձ����ڱڣ���ֹҺ�彦����
�ʴ�Ϊ��©���¶˼���δ�����ձ��ڱڣ�
��2��������Ӧ�ø��������Ӻ�笠����ӣ����ж��Ƿ�ϴ��������ȡ�������һ��ϴ��Һ������AgNO3��Һ���������ữ��AgNO3��Һ����Һ�����жϣ������ɰ�ɫ��������˵��û��ϴ�Ӹɾ�����û�г������ɣ���˵���Ѿ�ϴ�Ӹɾ������±��չ���Ӧ�������н��У�
�ʴ�Ϊ��AgNO3��Һ���������ữ��AgNO3��Һ����������
��3����ͼ3װ���Ʊ��Ȼ���ʱ������Ũ���������������A�з�Ӧ������������Ӧ�����ӷ���ʽΪMnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O�������Ȼ����ӷ��������Ƶõ����������Ȼ����ˮ������B�зű���NaCl��Һ����ȥ�����е��Ȼ��⣬C����Ũ���������ɵ��Ȼ�����ˮ�⣬��Ӧ��β��Ϊ������������������������������E��G֮���Fװ���з�Ũ�����ֹ����������Һ�е�ˮ����Eװ�ã�F��G������������������ˮ�������ü�ʯ�Ҵ��棬
�ʴ�Ϊ��MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O����ȥ�����е��Ȼ��⣻��ֹ����������Һ�е�ˮ����Eװ�ã���ʯ�ң�
��4��Cl2��Ca��OH��2��Ӧ�����Ȼ��ƺʹ�����ƣ���Ӧ�ķ���ʽΪ2Ca��OH��2+2Cl2�TCaCl2+Ca��ClO��2+2H2O��
�ʴ�Ϊ��2Ca��OH��2+2Cl2�TCaCl2+Ca��ClO��2+2H2O��
��5��Na2SO3��Һ����������������ԭ��Ӧ������������Ӻ������ӣ���Ӧ�����ӷ���ʽΪSO32-+Cl2+H2O�TSO42-+2Cl-+2H+��
�ʴ�Ϊ��SO32-+Cl2+H2O�TSO42-+2Cl-+2H+��
���� ���⿼�����ʵ��Ʊ�ʵ����ƣ���Ŀ�ѶȲ���ע�����ʵ����Ƶ���������˳�����ʵ��ԭ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�캣��ʡ������ѧ���¿�����ѧ�Ծ��������棩 ���ͣ�ʵ����
KAl(SO4)2��12H2O(����)��һ�ָ��Σ�����ֽ�ȷ���Ӧ�ù㷺��ʵ�����У����÷�������(��Ҫ�ɷ�ΪAl������������Fe��Mg����)�Ʊ������Ĺ�������ͼ��ʾ���ش��������⣺
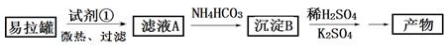
��1��Ϊ�������������ʣ��Լ���Ӧѡ�� (����)��
A��HCl��Һ B��H2SO4��Һ C����ˮ D��NaOH��Һ
��2�����ɳ���B�����ӷ���ʽΪ �����������ھ�ˮ����ԭ���� ����������Һ�еμ�Ba(OH)2��Һ��ǡ��ʹ��Һ�е�SO42-��ȫ���������ӷ���ʽΪ ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�캣��ʡ������ѧ���¿�����ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ����ȷ���� ( )
A����ҵ�ϴֹ���Ʊ���SiO2��C Si+CO2��
Si+CO2��
B��Cu2O��ϡH2SO4��Ӧ��Cu2O��2H+=2Cu+��H2O
C����ϡ����ϴ���Թ��ڱڵ�������3Ag+4H++NO3��=3Ag++NO��+2H2O
D .��Mg(HCO3)2��Һ�м������ռ���Һ:Mg2��+2HCO3��+2OH��=MgCO3��+2H2O+CO32��
.��Mg(HCO3)2��Һ�м������ռ���Һ:Mg2��+2HCO3��+2OH��=MgCO3��+2H2O+CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���������ʮ���и�����10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���ݺ����Ƽ�ԭ���Ʊ�����NaHCO3��ʵ�飬������ȡ��������ȡNaHCO3������NaHCO3������NaHCO3�ĸ����裬����ͼʾװ�ú�ԭ���ܴﵽʵ��Ŀ�ĵ���( )
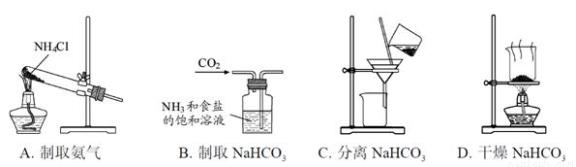
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���������ʮ���и�����10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���и������ӻ�����ܴ������棬��������Ӧ�Լ���ᷢ����ѧ�仯���ҷ�����Ӧ�����ӷ���ʽ��д������ȷ����
ѡ�� | ������ | �����Լ� | �����Լ�������Ӧ�����ӷ���ʽ |
A | Na����Fe3����Cl����I�� | NaOH��Һ | Fe3��+3OH��=Fe(OH)3�� |
B | Mg2����HCO | ����NaOH��Һ | Mg2����HCO H2O��Mg(OH)2����CO |
C | K����NH3��H2O��CO | ͨ������CO2 | 2OH����CO2=CO |
D | Na����NO | NaHSO4��Һ | SO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���Ŵ�����Ⱦ���������أ��������ڡ�ʮ���塱�ڼ䣬����������SO2���ŷ�������8%���������NOx���ŷ�������10%��Ŀǰ������������Ⱦ�ж��ַ�����
���Ŵ�����Ⱦ���������أ��������ڡ�ʮ���塱�ڼ䣬����������SO2���ŷ�������8%���������NOx���ŷ�������10%��Ŀǰ������������Ⱦ�ж��ַ�����Ũ��/mol•L-1 ʱ��/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com