
| |||||||||||
(1) |
分析:有关反应:H2+C12====2HCl HCl+NaOH==NaCl+H2O若Cl2有剩余,则还有: Cl2+2NaOH===NaCl+NaClO+H2O 解:若C12、H2恰好完全反应n(C12)=n(H2)= 若V(Cl2)<V(H2)Cl2最终全部转化为NaCl,n(NaC1)===(NaOH)=bmo1. 若n(C12)>n(H2)设H2物质的量为x,则有: H+Cl2===2HCl 1 1 2 X x 2x n(HCl)=n(NaCl)=2xmol C12+2NaOH===NaCl+NaClO+H2O 1 1 a-2x n(NaCl) n(NaCl)=(a-2x)mol 共生成,n(NaCl)=2x+(a-2x)=amol |
(2) |
解:由(1)题分析不难看出n(C12)= n(C12)> n(NaCl)=amol n(C12)=amol n(NaCl)=amol据此作图如下:
|


 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| △ |
| ||
| △ |
| 预期产物的相对分子质量 |
| 全部生成物质的相对分子质量总和 |
| a1V2 |
| 4a2(1-a1) |
| a1V2 |
| 4a2(1-a1) |
| 23V |
| 134.4 |
| 23V |
| 134.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 16 |
| a2 |
| 16 |
| a2 |
查看答案和解析>>
科目:高中化学 来源:2013届甘肃省河西五市部分普通高中高三第一次联合考试化学试卷(带解析) 题型:填空题
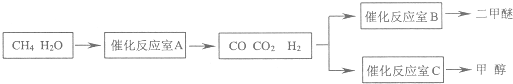
工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:
CO(g)+2H2(g) CH3OH(g) ΔH
CH3OH(g) ΔH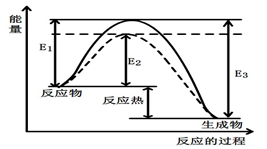
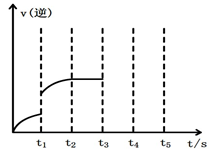
图1 (图中表示生成1mol物质时的能量) 图2
(1)根据图1请写出合成甲醇的热化学方程式
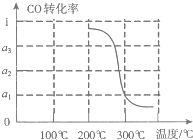
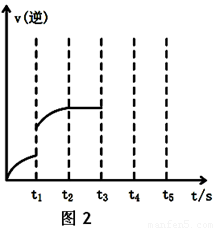
(2)该反应的逆反应速率随时间变化的关系如上图2。t1时改变了某种条件,改变的条件可能是 。
(3)判断反应达到平衡状态的依据是 (填字母序号)。
| A.2v(H2)(逆) =v(CO)(正) | B.混合气体的密度不变 |
| C.混合气体的平均相对分子质量不变 | D.CH3OH、CO、H2的浓度都不再发生变化 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省邯郸市高三教学质量检测理综化学试卷(解析版) 题型:填空题
工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:
CO(g)+2H2(g) CH3OH(g) ΔH
CH3OH(g) ΔH
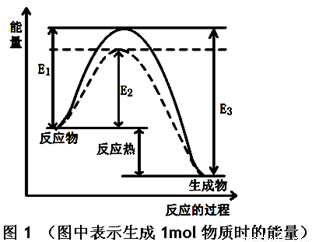
(1)根据图1请写出合成甲醇的热化学方程式
(热量用E1、E2或E3表示)。
(2)该反应的逆反应速率随时间变化的关系如上图2。t1时改变了某种条件,改变的条件可能是 。
(3)判断反应达到平衡状态的依据是 (填字母序号,下同)。
A. 2v(H2)(逆) =v(CO)(正)
B. 混合气体的密度不变
C. 混合气体的平均相对分子质量不变
D. CH3OH、CO、H2的浓度都不再发生变化
E.容器内CO、H2、CH3OH的浓度之比为1:2:1
(4)在一定温度下,若将4a mol H2和2amol CO放入2L的密闭容器中,充分反应后测得CO的转化率为50%,则该反应的平衡常数为 。若此时再向该容器中投入a mol CO、2amol H2和amol CH3OH,判断平衡移动的方向是 (“正向移动”“逆向移动”或“不移动”);与原平衡相比,CO的物质的量浓度 (填“增大”、“不变”或“减小”)。
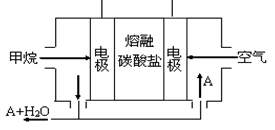
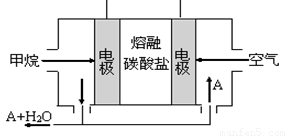
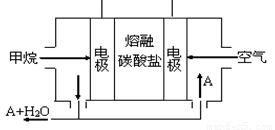
(5)某甲烷燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见右图)。A物质的化学式是_________;该原电池的负极反应式可表示为 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年甘肃省河西五市高三第一次联合考试化学试卷(解析版) 题型:填空题
工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:
CO(g)+2H2(g) CH3OH(g) ΔH
CH3OH(g) ΔH
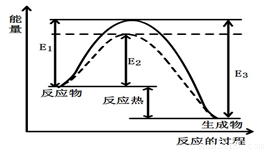
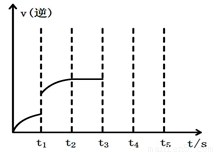
图1 (图中表示生成1mol物质时的能量) 图2
(1)根据图1请写出合成甲醇的热化学方程式
(2)该反应的逆反应速率随时间变化的关系如上图2。t1时改变了某种条件,改变的条件可能是 。
(3)判断反应达到平衡状态的依据是 (填字母序号)。
A.2v(H2)(逆) =v(CO)(正) B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.CH3OH、CO、H2的浓度都不再发生变化
E.容器内CO、H2、CH3OH的浓度之比为1:2:1
(4)在一定温度下,若将4a mol H2和2amol CO放入2L的密闭容器中,充分反应后测得CO的转化率为50%,则该反应的平衡常数为 。若此时再向该容器中投入a mol CO、2amol H2和amol CH3OH,判断平衡移动的方向是 (“正向移动”“逆向移动”或“不移动”);与原平衡相比,CO的物质的量浓度 (填“增大”、“不变”或“减小”)。
(5)某甲烷燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见图)。A物质的化学式是_________;该原电池的负极反应式可表示为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com